
| A. | 极性键 | B. | 非极性键 | C. | 离子键 | D. | 氢键 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②④⑤ | C. | ①③④ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰融化时,分子中H-O键发生断裂 | |
| B. | 由于H-O键比H-S键牢固,所以水的熔沸点比H2S高 | |
| C. | 在由分子所构成的物质中,分子间作用力越大,该物质越稳定 | |
| D. | 随着电子层数的增加,卤单质X2分子间作用力逐渐增大,熔沸点逐渐升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
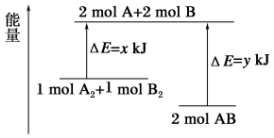
| A. | 该反应是吸热反应 | |
| B. | 断裂1molA-A键和1molB-B键可放出X kJ的能量 | |
| C. | 2molAB的总能量高于1molA2和1molB2的总能量 | |
| D. | 断裂2molA-B键需吸收YKJ的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
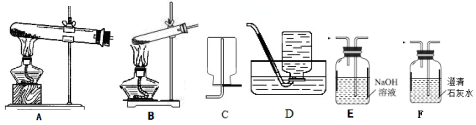
| 试管 | A | B | C |
加入试剂 | 4mL 0.01mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 | 4mL 0.02mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 | 4mL 0.03mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 |
| 褪色时间 | 28秒 | 30秒 | 不褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验溴乙烷中是否有溴元素,方法是先加入NaOH溶液共热,冷却后用过量稀硝酸中和过量碱,再加硝酸银溶液,观察有无浅黄色沉淀生成 | |
| B. | 卤代烃水解后的有机产物一定为醇 | |
| C. | 所有卤代烃在适当条件下都能发生消去反应 | |
| D. | 所有卤代烃都是通过取代反应制得的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com