
【题目】(1)某温度(t℃)时,测得0.01mol/L的NaOH溶液的pH=11,则该温度下水的KW=_______。在此温度下,将pH=a的NaOH溶液Va L与pH=b的H2SO4溶液Vb L混合,若所得混合液为中性,且a+b=12,则Va:Vb=___________。
(2)25℃时,0.1mol/L的HaA溶液中c(H+)/c(OH-)=1010,请回答下列问题:
①HaA是___________(填“强电解质”或“弱电解质”)。
②在加水稀释HaA溶液的过程中,随着水量的增加而增大的是__________(填字母)
A.c(HaA) B.c(H+)/c(HaA) C.c(H+)与c(OH-)的乘积 D.c(OH-)
③NanA溶液显__________(填“酸性”、“中性”或“碱性”),理由是(用离子方程式表示)____________。
【答案】(1)1×10-13; 10:1;
(2)①弱电解质;②bd③碱性 An++H2O![]() HA(n-1)++OH-。
HA(n-1)++OH-。
【解析】
试题分析:(1)某温度(t℃)时,测得0.01mol/L的NaOH溶液的pH=11,c(H+)=10-11mol/L,c(OH-)=0.01mol/L,则Kw= c(H+) c(OH-)=10-11mol/L×0.01mol/L= 1×10-13(mol/L)2;某温度(t℃)时,测得0.01molL-1的NaOH溶液的pH=11,据此计算离子积常数Kw=0.01mol/L×10^-11 mol/L=10-13(mol/L),将pH=2的H2SO4溶液VaL与pH=12的NaOH溶液Vb L混合,若所得混合液为中性说明氢离子和氢氧根离子物质的量相同,10-2×Va=(1013/1012)×Vb,得到Va:Vb=10:1;(2)25℃时,0.1mol/L的HaA溶液中c(H+)/c(OH-)=1010,由于该温度下Kw= c(H+)c(OH-)=1×10-14;则c(H+)=0.01mol/L<c(HaA)=0.1mol/L,①HaA是弱酸,即该物质是弱电解质。②在加水稀释HaA溶液的过程中,HaA![]() H++Ha-1A-,加水稀释,电离平衡正向移动,酸电离产生的H+、Ha-1A-的物质的量增大,由于稀释作用大于平衡正向移动,c(HaA)减小;选项a错误;c(H+)、c(HaA)都减小,由于c(HaA)减小的倍数大于c(H+),所以c(H+)/c(HaA)增大,选项b正确;所以随着水量的增加溶液中c(H+)减小,由于温度不变,Kw= c(H+)与c(OH-)的乘积不变;所以c(OH-)增大;选项c错误,选项d正确;NaaA是强碱弱酸盐,在溶液中Aa-水解消耗水电离产生的氢离子,所以使溶液中c(H+)<c(OH-),所以溶液显碱性,用离子方程式表示为Aa++H2O
H++Ha-1A-,加水稀释,电离平衡正向移动,酸电离产生的H+、Ha-1A-的物质的量增大,由于稀释作用大于平衡正向移动,c(HaA)减小;选项a错误;c(H+)、c(HaA)都减小,由于c(HaA)减小的倍数大于c(H+),所以c(H+)/c(HaA)增大,选项b正确;所以随着水量的增加溶液中c(H+)减小,由于温度不变,Kw= c(H+)与c(OH-)的乘积不变;所以c(OH-)增大;选项c错误,选项d正确;NaaA是强碱弱酸盐,在溶液中Aa-水解消耗水电离产生的氢离子,所以使溶液中c(H+)<c(OH-),所以溶液显碱性,用离子方程式表示为Aa++H2O![]() HA(a-1)++OH-。
HA(a-1)++OH-。


科目:高中化学 来源: 题型:
【题目】下列有关物质的性质和用途具有对应关系的是
A. SO2具有氧化性,可用于漂白纸浆
B. CO具有还原性,可用于冶炼铁等金属
C. SiO2熔点高,可用作光导纤维
D. Al2O3具有两性,可用作耐高温材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】12.8 g铜和浓HNO3反应,随反应进行,产生气体的颜色逐渐变浅,铜完全反应时,收集到标准状况下的气体6.72 L,将气体与一定体积的O2同时通入水中可被完全吸收。
(1)通过计算确定收集到的气体成分及物质的量。
(2)O2在标准状况下的体积。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu。

(1)将上述反应设计成的原电池如图甲所示,请回答下列问题:
①图中X溶液是 ;②Cu电极上发生的电极反应式为 ;
③原电池工作时,盐桥中的 离子(填“K+”或“Cl—”)不断进入X溶液中。
(2)将上述反应设计成的电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题:
①M是 极;②图丙中的②线是 离子的变化。
③当电子转移为2mol时,向乙烧杯中加入 L 5mol·L-1NaOH溶液才能使所有的金属阳离子沉淀完全。
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O![]() Na2FeO4+3H2↑,则电解时阳极的电极反应式是 。
Na2FeO4+3H2↑,则电解时阳极的电极反应式是 。
②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为 。
③Na2FeO4能消毒、净水的原因 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(有机化学基础)OPA可用作内窥镜手术用器械抗菌消毒剂,也用于合成新抗血小板聚集药吲哚波芬。由烃A合成OPA的转化关系如图所示。

已知:无a –H(醛基相邻碳上的氢)的醛能发生歧化反应,如:2HCHO+KOH![]() CH3OH+HCOOK
CH3OH+HCOOK
回答下列问题:
(2)下列关于A的说法正确的是__________(填字母)。
a.与苯互为同系物 b.能与溴水发生加成反应
c.能使酸性高锰酸钾溶液褪色 d.能发生加聚反应生成高分子化合物
(2)A→B的反应类型为___________。
(3)OPA的化学名称为____________。
(4)C中所含官能团的名称为__________。
(5)E是一种聚醋类高分子化合物,由D生成E的化学方程式为___________。
(6)D的同分异构体中,含有苯环且苯环上只有两个取代基,能水解且能与FeC13 溶液发生显色反应的有___________种,其中能发生银镜反应且核磁共振氢谱只有5组峰的是_________(填结构简式)。
(7)写出以甲苯为原料(其他无机试剂任选)制备苯甲酸苯甲醋的合成路线:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是
A.υ(W)=3υ(Z)
B. 3υ(X)=2υ(Z)
C.υ(X)= 2υ(Y)
D. 3υ(W)=2υ(X)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)已知磷酸(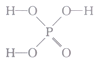 )分子中的三个氢原子都可以与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2) 却不能与D2O发生氢交换。则H3PO2是(填“一元”“二元”或“三元”)酸,其分子的结构式为________(填字母)。
)分子中的三个氢原子都可以与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2) 却不能与D2O发生氢交换。则H3PO2是(填“一元”“二元”或“三元”)酸,其分子的结构式为________(填字母)。

(2)H3PO2具有较强的还原性,可以通过电解的方法制备。“四室电渗析法”工作原理如图所示(阳离子交换膜和阴离子交换膜分别只允许阳离子、阴离子通过)。

①阳极的电极反应式为_________。
②II 膜为___________(填“阴离子交换膜”或“阳离子交换膜”)。
③早期采用“三室电渗析法”制备H3PO2,将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的交换膜,从而合并阳极室与产品室,其缺点是产品中混有______杂质。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com