
对化学反应的限度的叙述,错误的是( )
A.任何可逆反应都有一定的限度
B.化学反应达到限度时,正、逆反应速率相等
C.化学反应的限度与时间的长短无关
D.化学反应的限度是不可改变的
科目:高中化学 来源:2015-2016学年江苏省高二下期中化学试卷(解析版) 题型:选择题
如下图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动)。下列叙述正确的是

A.a中铁钉附近呈现红色 B.b中铁钉上发生还原反应
C.a中铜丝上发生还原反应 D.b铁钉上有气泡产生
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林长春外国语高一下期中理科化学试卷(解析版) 题型:填空题
50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
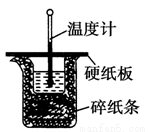
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是________。
(2)烧杯间填满碎泡沫塑料的作用是_________________________。
(3)理论上稀的强酸溶液与强碱溶液反应生成1 mol水时放出57.3 kJ的热量,写出表示稀盐酸和稀氢氧化钠溶液反应的中和热的热化学方程式:_______________。
(4)大烧杯上如不盖硬纸板,求得的中和热数值______(填“偏大”、“偏小”或“无影响”)。
(5)实验中改用60 mL 0.50 m ol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量__________(填“相等”或“不相等”),所求中和热__________(填“相等”或“不相等”),简述理由:________________________________________________。
ol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量__________(填“相等”或“不相等”),所求中和热__________(填“相等”或“不相等”),简述理由:________________________________________________。
(6)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会____________(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林长春外国语高一下期中理科化学试卷(解析版) 题型:选择题
美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数为118、质量数为293的
超重元素,该元素原子的中子数为( )
A. 118 B. 175 C. 47 D. 293
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林长春外国语高一下期中理科化学试卷(解析版) 题型:选择题
如图,小烧杯放在一块沾有水的玻璃片上,加入NH4Cl固体与氢氧化钡晶体[ Ba(OH)2·8H2O],并用玻璃棒搅拌,玻璃片上的水结成了冰。由此可推断( )
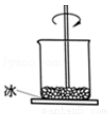
A. 该反应中,化学能转变成热能
B. 反应物的总能量低于生成物的总能量
C. 氯化铵与氢氧化钡的反应为放热反应
D. 反应的热化学方程式为:2NH4Cl+Ba(OH)2=BaCl2+2NH3·H2O ΔH<0
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州凯里一中高一下期中文科化学试卷(解析版) 题型:选择题
下列各组材料中不能组成原电池的是( )
A.锌片、石墨、硫酸溶液 B.铜片、银片、氯化铁溶液
C.锌片、铜片、乙醇溶液 D.铁片、铜片、稀盐酸
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州凯里一中高一下期中文科化学试卷(解析版) 题型:选择题
下列说法中,错误的是( )
A.人类目前所直接利用的能量大部分是由化学反应产生的
B.煤、石油、天然气是当今世界最重要的三种化石燃料
C.我国目前最主要的能源是煤炭
D.人体运动所消耗的能量与化学反应无关
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州凯里一中高一下期中文科化学试卷(解析版) 题型:选择题
下列关于化学键说法中不正确的是( )
A.化学键是一种作用力
B.化学键可以使离子相结合,也可以使原子相结合
C.化学反应过程中,反应物化学键的断裂,生成物化学键的形成
D.非极性键不是化学键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西桂林十八学高二下期中化学试卷(解析版) 题型:填空题
氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:

 (1)氢氧燃料电池的
(1)氢氧燃料电池的 能量转化主要形式是 ,在导线中电子流动方向为
能量转化主要形式是 ,在导线中电子流动方向为  (用a、b 表示)。
(用a、b 表示)。
 (2)负极反应式为 。
(2)负极反应式为 。
 (3)电极表面镀铂粉的原因是 。
(3)电极表面镀铂粉的原因是 。
 (4)该电池工作时,H2和O2连续由外部供给,电池可连续不断
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断
提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:w.w.w.manfen5.c.o.m Ⅰ.2Li+H2
Ⅰ.2Li+H2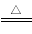 2LiH
2LiH Ⅱ.LiH+H2O=
Ⅱ.LiH+H2O= LiOH+H2↑
LiOH+H2↑
 ①反应Ⅱ中的氧化剂是 。
①反应Ⅱ中的氧化剂是 。
 ②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
 ③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 mol。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com