
下列说法错误的是
A.使用如图所示装置验证Ka(CH3COOH)>Ka(H2CO3)>Ka(H2SiO3)
B.0.1 mol·L-1的醋酸中加入水或加入冰醋酸均可使醋酸电离平衡向电离方向移动
C.等物质的量浓度的CH3COONa和Na2CO3溶液,后者溶液中水的电离程度大
D.等pH的醋酸和碳酸,分别加水稀释后溶液的pH仍相等,则醋酸中加入水的体积少
科目:高中化学 来源: 题型:
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如图所示,则下列说法中错误的是
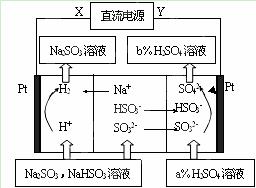
A.X为直流电的负极,Y为直流电的正极
B.图中两处硫酸的质量分数b>a
C.该过程中的产品主要为H2SO4和H2
D.阳极区pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述不正确的是
A.在实验室里硅酸钠溶液存放在带橡胶塞的试剂瓶中
B.提倡人们购物时不用塑料袋,是为了防止白色污染
C.氟利昂(CCl2F2)因破坏大气臭氧层而导致“温室效应”
D.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中放入甲、乙、丙、丁四种物质,一段时间后测得数据如下:
| 四种物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 25 | 15 | 1 | 5 |
| 反应后质量(g) | 11 | 未测 | 1 | 22 |
则下列表述正确的是
A. 未测值为3 g B.丙一定是催化剂
C.乙全部参加反应 D.甲与乙反应的质量比为14∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
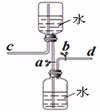
右图是某同学设计的储气装置(固定装置已略去),下列说法中,不正确的是
A.打开止水夹a、b,气体从d管导入,储存在下面的集气瓶里
B.取用储存在下面集气瓶里的气体时,通过控制止水夹a、b,
可将气体顺利排出
C.气体被储存在下面的集气瓶里时,c导管也必须安装止水夹
D.该装置也可作为制取二氧化碳气体的发生装置
查看答案和解析>>
科目:高中化学 来源: 题型:
甲是一种盐,由A、B、C、D、E五种元素组成,其中四种是短周期元素。甲溶于水后可电离出由上述元素组成的三种离子,其中含有由A、B形成的10电子阳离子。A元素原子核内质子数比E的少1,D、E处于同主族。
用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中加入适量NaOH溶液,加热;
③取少量甲溶液于试管中滴入KSCN溶液,无现象,再滴入氯水,溶液呈红色;
④取少量甲溶液于试管中,向其中加入稀盐酸,再加入BaCl2溶液,出现白色沉淀。
回答下列问题:
(1)C在周期表中的位置 。
(2)实验②中出现的现象是 。
(3)用离子方程式表示实验③中现象的原因: ;若向此时溶液中加入KCl溶液,此溶液中的平衡(非水的电离平衡及盐的水解平衡)将 (填 “不移”,“左移”,“右移”)。
(4)由A、B、D、E组成的阳阴粒子个数比为1:2的盐X,在X的水溶液中,c(H+)==________________。
(5)经测定甲晶体的摩尔质量为392 g/mol,其中阳离子与阴离子物质的量之比为3:2,则甲晶体的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中物质的量浓度为1 mol·L-1的是( )。
A.将40 g NaOH固体溶解于1L水中
B.将22.4 L氯化氢气体溶于水配成1L溶液
C.将1L 10 mol·L-1的浓盐酸与9 L水混合
D.10 g NaOH固体溶解在水中配成250 mL溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.标准状况下,11.2 L NH3溶于1 L水,溶液中含有N原子的微粒总数为0.6NA
B.1.00 mol NaCl中,所有Na+的最外层电子总数约为8×6.02×1023
C.欲配制1.00 L 1.00 mol·L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中
D.1mol FeCl3完全转化为Fe(OH)3胶体后形成NA个胶粒.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com