
【题目】短周期主族元素X、Y、Z、R、T的原子半径与原子序数关系如下图所示。R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的化合物Z2T能破坏水的电离平衡。下列推断正确的是

A. 原子半径和离子半径均满足:Y<Z
B. 氢化物的沸点不一定是:Y>R
C. 最高价氧化物对应水化物的酸性:T<R
D. 由X、R、Y、Z四种元素组成的化合物水溶液一定显碱性
【答案】B
【解析】R原子最外层电子数是电子层数的2倍,可能为C或S,由于图示原子半径和原子序数关系可知R应为C;Y与Z能形成Z2Y、Z2Y2型离子化合物,应为Na2O、Na2O2,则Y为O,Z为Na;Z与T形成的Z2T化合物能破坏水的电离平衡,T应为S,Na2S水解呈碱性,可促进水的电离;X的原子半径最小,原子序数最小,应为H元素。A.原子半径O<Na,离子半径O2->Na+,故A错误;B.R为C,对应的氢化物为烃,如含碳原子数较多,常温下为固体,沸点较高,则氢化物的沸点不一定是:Y>R,故B正确;C.非金属性S>C,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故C错误;D.由H、C、O、Na四种元素组成的化合物不仅仅为NaHCO3,可能为有机盐且含有羧基,溶液不一定为碱性,可能为酸性,故D错误;故选B。


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】下列有关物质性质与应用叙述正确的是
A. 浓硫酸具有吸水性,可用于干燥氨气、二氧化碳等气体
B. 碳酸钠溶液有碱性,是治疗胃酸过多的一种药剂
C. SO2具有漂白性,可用于漂白食用粉丝、银耳等物质
D. 浓硫酸具有强氧化性,可用铁制容器存放浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组以石膏(CaSO4·2H2O)为主要原料制备(NH4)2SO4的流程如下:

下列说法正确的是( )
A. 气体B是NH3,可循环利用
B. 操作Ⅰ中,所用的主要玻璃仪器为烧杯、玻璃棒、分液漏斗
C. 操作Ⅱ中,可用蒸发结晶的方法得到纯净的(NH4)2SO4
D. 整个过程的总反应方程式为CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【选修5——有机化学基础】
某新型有机化学材料G的合成路线如图所示,请回答下列问题:
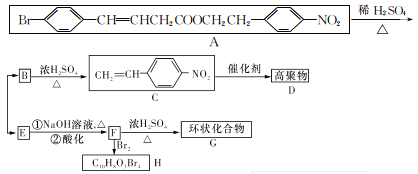
(1)F分子中的含氧官能团名称为_______。
(2)高聚物D的结构简式是_______。
(3)写出反应A→B+E的化学方程式:________。
(4)F→H的反应类型有______、_________。
(5)B的同分异构体有多种,其中官能团种类不变,能与FeCl3溶液发生显色反应,核磁共振氢谱显示有6组峰,且峰面积之比为1:1:1: l:2:3的同分异构体有_____种。
(6)参照上述合成路线,以CH3CHBrCOOCH3为原料(无机试剂任选),设计制备聚乳酸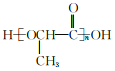 的合成路线_____________________。
的合成路线_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置(熔融CaF2-CaO作电解质)获得金属钙,并用钙还原TiO2制备金属钛。下列说法正确的是

A. 电解过程中,Ca2+向阳极移动
B. 阳极的电极反应式为: C+2O2--4e-=CO2↑
C. 在制备金属钛前后,整套装置中CaO的总量减少
D. 若用铅蓄电池作该装置的供电电源,“+”接线柱连接的是Pb电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的5种物质中均含同种金属元素,且在一定条件下(不含电解)能按图示箭头方向实现一步转化,则该金属元素可能是

①Na②K③Ca④Fe⑤Cu
A. ①② B. ③④ C. ④⑤ D. ①⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com