
某化学实验兴趣小组同学向用大理石和稀盐酸制备CO2后残留液中滴加碳酸钠溶液,在溶液中插入pH传感器,测得pH变化曲线如图所示,下列有关说法不正确的是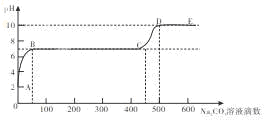
| A.开始时溶液pH=2是因为残留液中还有盐酸剩余 |
| B.AB段表示随着碳酸钠溶液的滴入,CaCO3沉淀的质量逐渐增加 |
| C.BC段发生的反应为:Ca2++CO32-= CaCO3↓ |
| D.滴入500滴碳酸钠溶液后溶液中c(OH-)>c(H+) |
科目:高中化学 来源: 题型:单选题
下列离子方程式中,属于水解反应的是
A.HCOOH+H2O HCOO-+H3O+ HCOO-+H3O+ | B.CO2+H2O HCO-3+H+ HCO-3+H+ |
C.CO32-+ H2O HCO-3+OH- HCO-3+OH- | D.HS- S2-+H+ S2-+H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列电解质溶液的有关叙述正确的是
| A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 |
| B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH >7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C.用0.2000 mol/L NaOH标准溶液滴定HCI与CH3COOH的混合液(混合液中两种酸的浓度均约为0.1 mol/L),至中性时,溶液中的酸未被完全中和 |
| D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水②0.1mol/L盐酸③0.1 mol/L氯化镁溶液④0.1 mol/L硝酸银溶液中,Ag+浓度:①>④=②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.常温下,将pH=11的氨水稀释到原体积的10倍后,溶液的pH=10 |
| B.为确定某酸.H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C.用0.2000 mol/L NaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合液中两种酸的浓度均约为0.1mol/L),至中性时,溶液中的酸未被完全中和 |
| D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水②0.1 mol/L盐酸 ③0.1 mol/L氯化镁溶液④0.1 mol/L硝酸银溶液中,则Ag+浓度:①>④=②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下将一定浓度的一元酸HA和0.1 mol·L-1NaOH溶液等体积混合后,下列说法正确的是
A.若pH=7,HA的浓度一定为0.1 mol·L-1
B.若pH>7,HA的pH不可能等于1
C.若pH<7,溶液中的微粒浓度关系为: c(Na+)=c(HA)+c(A-)
D.若pH=12,且HA为强酸时,HA的浓度应为0.08 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知常温时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=12.0,则下列说法不正确的是 ( )
| A.所得溶液中的c(H+)=1.0×10-12 mol·L-1 |
| B.所加的烧碱溶液pH=12.0 |
| C.所得溶液中由水电离产生的c(OH-)=1.0×10-12 mol·L-1 |
| D.所得溶液中的c(Mg2+)=5.6×10-8 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知温度T时,水的离子积常数为KW,该温度下将V1mLa mol?L-1的一元酸HA与V2mLb mol?L-1的一元碱BOH充分混合,下列判断一定正确的是
A.若V1a=V2b,稀释此混合溶液时,溶液中各离子浓度一定都发生变化
B.若pH(HA)+ pH(BOH)=14,则V1=V2时,酸碱恰好完全中和
C.此混合液中:2c(H+)+c(B+)≤c(OH-)+c(A-)
D.若混合溶液中c(OH-)=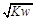 mol?L-1,则此溶液一定呈中性
mol?L-1,则此溶液一定呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知Ksp(BaSO4 )= 1.1×10-10,Ksp(BaCO3)=2.5×10-9。下列说法中不正确的是
| A.BaSO4比BaCO3溶解度小,所以,BaCO3可以转化为BaSO4 |
| B.BaCO3、BaSO4均不溶于水,所以都可以做钡餐试剂 |
| C.向Na2CO3溶液中加入BaCl2和Na2SO4,当两种沉淀共存时,c(SO42—)/ c(CO32—) =4.4×10-2 |
| D.常温下,BaCO3若要在Na2SO4溶液中开始转化为BaSO4,则Na2SO4的浓度必须不低于 2.2×10-6 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述正确的是
| A.将pH=2的盐酸和pH=2的醋酸等体积混合,混合后溶液的pH=2 |
| B.HA-比HB-更难电离,则NaHA溶液的pH一定比NaHB溶液的大 |
| C.在饱和氨水中加入同浓度的氨水,平衡正向移动 |
| D.某温度下,Ba(OH)2溶液中,Kw=10-12,pH=8的该溶液中加入等体积pH=4的盐酸,混合溶液的pH=7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com