
 ,故答案为:
,故答案为: ;Fe(OH)2;
;Fe(OH)2;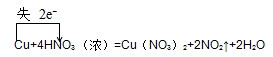 ,该反应的氧化剂和还原剂的物质的量之比为2:1,
,该反应的氧化剂和还原剂的物质的量之比为2:1,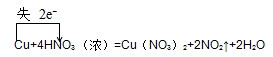 ;2:1;
;2:1;

科目:高中化学 来源: 题型:
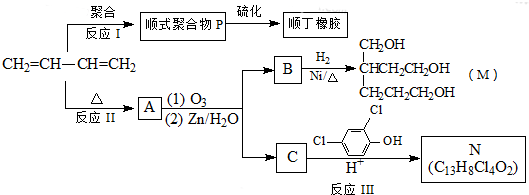
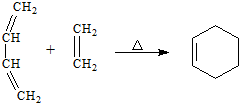
| (1)O3 |
| (2)Zn/H2O |
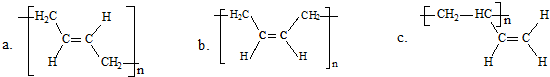
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 2 |
2+ 2 |
2+ 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
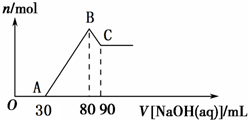 Ⅰ.短周期元素R被称为“生命元素”,R元素的最价高氧化物对应的水化物能与其气态氢化物化合生成盐A,写出生成A的化学方程式
Ⅰ.短周期元素R被称为“生命元素”,R元素的最价高氧化物对应的水化物能与其气态氢化物化合生成盐A,写出生成A的化学方程式查看答案和解析>>
科目:高中化学 来源: 题型:
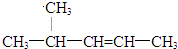 ⑤间甲基苯乙烯
⑤间甲基苯乙烯 查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、上述两个反应中反应物的总能量均大于生成物的总能量 |
| B、上述两个反应中反应物的总能量均小于生成物的总能量 |
| C、H2(g)和Cl2(g)反应生成1 mol HCl(g)时放出Q1kJ的热量 |
| D、1molHBr(g)具有的能量大于1molHBr(l)具有的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N60易溶于水 |
| B、N60是N2的一种同素异形体 |
| C、等物质的量分解吸收的热量N60>N2 |
| D、N60是共价键结合的空心球状结构 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com