
【题目】某研究性学习小组将下列装置如图连接,E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:

(1)电源A极的名称是____,丁中____(填“X”或“Y”)极颜色会加深。
(2)欲用丙装置给铜镀银,H应该是____,电镀液的主要成分是____(填化学式)。
(3)如果收集乙装置中产生的气体,相同条件下两种气体的体积比是___。
(4)甲装置为使用过的铅蓄电池,充电后电极D应与用电器的____(填“正”或“负”)极连接,电极C上的电极反应式为____。
【答案】正极 Y Cu AgNO3 1:1 负 PbSO4 - 2e-+ 2H2O = PbO2 + SO42-+ 4H+
【解析】
将电源接通后,向乙中滴入酚酞试液,在F极附近显红色,说明F极生成OH-,则F为阴极,因此电源的A为正极,B为负极,C、E、G、X为阳极,D、F、H、Y为阴极,结合电解原理和胶体的电泳分析解答。
根据上述分析,A为正极,B为负极,C、E、G、X为阳极,D、F、H、Y为阴极。
(1)A是电源的正极,B是电源的负极;根据异性电荷相吸的原理,氢氧化铁胶体中含有的带正电荷的胶体粒子会向阴极即Y极移动,所以Y极附近红褐色变深,故答案为:正极;Y;
(2)给铜镀银,应该选用金属银作阳极,纯铜作阴极,含有银离子的硝酸银溶液作电解质溶液,即H为纯铜,电镀液的主要成分是AgNO3,故答案为:Cu;AgNO3;
(3)电解饱和食盐水的原理是:2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑,相同条件下,产生的氢气和氯气体积比为1∶1,故答案为:1∶1;
2NaOH+H2↑+Cl2↑,相同条件下,产生的氢气和氯气体积比为1∶1,故答案为:1∶1;
(4)甲装置为使用过的铅蓄电池,充电后电极D为负极,使用时应与用电器的负极连接,电极C为阳极,发生氧化反应,电极反应式为PbSO4 - 2e-+ 2H2O = PbO2 + SO42-+ 4H+,故答案为:负;PbSO4 - 2e-+ 2H2O = PbO2 + SO42-+ 4H+。


科目:高中化学 来源: 题型:
【题目】如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2和O2的混合气体,在标准状态下,若将H2、O2的混合气体点燃引爆。活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来H2、O2的体积之比可能为( )
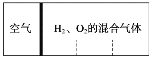
A. 2∶7B. 5∶4C. 4∶5D. 2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜类化合物广泛存在于动植物体内。下列关于萜类化合物a、b的说法正确的是
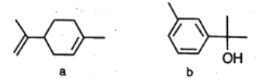
A.a中六元环上的一氯代物共有3种(不考虑立体异构)
B.a分子中所有原子都可能共平面,b的分子式为C10H12O
C.a和b都能发生加成反应、氧化反应、取代反应
D.1 mol b与足量的钠反应产生1 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是

A. 向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B. 实验中装置b中的液体逐渐变为浅红色
C. 装置c中的碳酸钠溶液的作用是吸收溴化氢
D. 反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年4月26日,中田首艘国产航母在大连正式下水,标志着我国自主设计航空母舰取得重大阶段性成果。请回答下列问题:
(1)航母用钢可由低硅生铁冶炼而成。
①硅原子L能层的电子分布图为____________________;
②Fe3+比Fe2+稳定的原因是_____________________;
③铁氰化钾K3[Fe(CN)6]溶液可以检验Fe2+。1 mol CN-中含有π键的数为_________,与CN-互为等电子体的分子有__________(写出一种),铁氰化钾晶体中各种微粒间相互作用不包括_______________;
a. 离子键 b. 共价键 c.配位键 d. 金属键 e. 氢键 f. 范德华力
(2)航母螺旋桨主要用铜合金制造。含铜废液可以利用铜萃取剂M,通过如下反应实现铜离子的富集,进行回收。

①M所含元素的电负性由大到小的顺序为__________(用元素符号表示);
②X中采用sp3杂化的非金属原子有___________(填写元素名称),采用sp3杂化的原子有__________个;
(3)Fe3O4是Fe3+、Fe2+、O2-通过离子键而组成的复杂离子晶体。O2-的重复排列方式如图所示,已知该晶体的晶胞参数为a nm,密度为b g/cm3,则NA=__________mol-1。(列出含a、b的计算式)
 (白球表示O2-)
(白球表示O2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物H(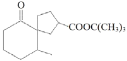 )是一种用于合成健脾,祛风,散寒药物的中间体,其合成路线如下:
)是一种用于合成健脾,祛风,散寒药物的中间体,其合成路线如下:

已知:①![]()
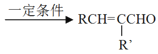 +H2O(R,
+H2O(R,![]() 是H或烃基)
是H或烃基)
②![]()
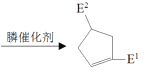 (
(![]() 可以是
可以是![]() 或
或![]() )
)
回答下列问题:
(1)A含有的官能团是__________________________________;
(2)B的结构简式为__________________________________;
(3)将下列B→C的多步反应流程图补充完整(标明反应条件):
_____________________________________________;
(4)由C和D生成E的化学方程式为_______________________________________;
(5)下列说法正确的是_______________________;
a.物质D的核磁共振氢谱有2组吸收峰;
b.物质F可与FeCl3溶液发生显色反应;
c.G→H的反应为加成反应;
(6)E和F反应生成G的化学方程式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
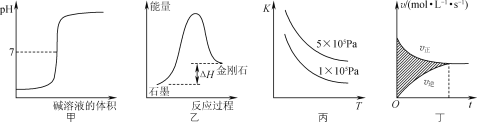
A. 图甲所示,表示强碱滴定强酸的滴定曲线
B. 图乙所示,从能量角度考虑,金刚石比石墨稳定
C. 图丙所示,表示反应2SO2(g)+O2(g)![]() 2SO3(g);ΔH<0的平衡常数K与温度和压强的关系
2SO3(g);ΔH<0的平衡常数K与温度和压强的关系
D. 图丁所示,图中的阴影部分面积的含义是[υ(正)-υ(逆)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于乙炔分子中的共价键说法正确的是
A. sp杂化轨道形成σ键属于极性键,未杂化的2p轨道形成π键属于非极性键
B. C-H之间是sp-s形成σ键,与s-p σ键的对称性不同
C. (CN)2与乙炔都属于直线型分子,所以(CN)2分子中含有3个σ键和2个π键
D. 由于π键的键能比σ键的键能小,乙炔分子![]() 三键的键能小于C-C单键的键能的3倍,所以乙炔化学性质活泼易于发生加成反应
三键的键能小于C-C单键的键能的3倍,所以乙炔化学性质活泼易于发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
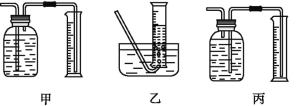
【题目】如图是铁与水蒸气反应的实验装置。在硬质玻璃管中放入还原铁粉和石棉绒(石棉绒是耐高温材料,与水、铁不反应)的混合物,加热,并通入水蒸气,就可以完成高温下铁与水蒸气反应的实验。
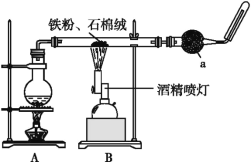
(1)已知该实验反应的反应方程式为:Fe+H2O![]() Fe3O4+H2(请配平)____。
Fe3O4+H2(请配平)____。
(2)仪器a的名称是________。
(3)某同学为了研究一定时间内铁粉的转化率,设计了如下实验:准确称量一定质量的铁粉进行反应,测量反应后生成气体的体积,计算铁粉的转化率。
①该同学应该先点燃___(填“A”或“B”)处的酒精灯(或酒精喷灯),测量气体体积不可以选用上图中___(填“甲”“乙”或“丙”)装置。
②称取5.6 g铁粉与适量石棉绒混合,然后加热反应一段时间。若测出的气体体积在标准状况下为0.448 L,则铁粉的转化率为___。
(4)将硬质玻璃管中反应后的固体混合物全部取出置于烧杯中,加入足量的盐酸溶解并过滤,为探究反应后溶液中可能的阳离子,小林同学进行如下实验,请你将下表补充完整:
步骤 | 现象 | 解释(用离子方程式表示) | 结论 |
Ⅰ.取样,滴加KSCN溶液 | 溶液不变红色 | ①Fe3O4+8H+=Fe2++2Fe3++4H2O ②____________ | Ⅲ.反应后的溶液中阳离子为_______ |
Ⅱ.取样,滴加NaOH溶液 | 刚开始无明显现象,一段时间后先出现白色沉淀,迅速变为灰绿色,最终变为红褐色 | ①____________ ②Fe2++2OH—=Fe(OH)2↓ ③4Fe(OH)2+2H2O+O2=4Fe(OH)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com