
 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
(1)9.2g氮的氧化物NOx中含有N原子数为0.2 mol,
则NOx的摩尔质量为___________,x数值为_______,
这些质量的NOx在标准状况的体积约为_______。
(2)V L Fe2(SO4)3溶液中含有a g SO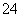 ,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为_________________
,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
第3周期元素的基态原子中,不可能出现d电子,主要依据是
A.能量守恒原理 B.泡利不相容原理
C.洪特规则 D.近似能级图中的顺序3d轨道能量比4s轨道高
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家一直致力于研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、N2、压强1.0×105 Pa、反应时间3 h):
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量 /10-6 mol | 4.8 | 5.9 | 6.0 | 2.0 |
相应的热化学方程式如下:N2(g)+3H2O(l)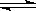 2NH3(g)+
2NH3(g)+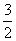 O2(g)
O2(g)
ΔH=+765.2 kJ·mol-1
回答下列问题:(1)请画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化的示意图,并进行必要标注。
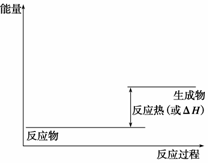
(2)与目前广泛使用的工业合成氨方法相比,该方法固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议:(写两点)
_______________________________;____________________________________。
(3)工业合成氨的反应为N2(g)+3H2(g) 2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为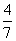 。计算:①该条件下N2的平衡转化率为 (保留一位小数)。
。计算:①该条件下N2的平衡转化率为 (保留一位小数)。
②该条件下反应2NH3(g) N2(g)+3H2(g)的平衡常数 。
N2(g)+3H2(g)的平衡常数 。
③若反应温度不变,假如在容积为2.0 L的密闭容器中起始充入0.40 mol N2(g)和0.40 mol H2(g),反应3min时测得体系压强为原来的3/4,这段时间H2的平均反应速率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某烃结构简式如右图,则该有机物应命名为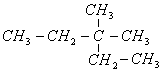
A. 2—甲基 — 2 — 乙基丁烷 B. 3 — 甲基 — 3 — 乙基己烷
C. 2,2 — 二甲基戊烷 D. 3,3 — 二甲基戊烷
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:25 ℃时,Ksp[Mg(OH)2]=5.61×10-12,Ksp[MgF2]=7.42×10-11 。则25 ℃条件下,下列说法正确的是
A.饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大
B.在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大
C. Mg(OH)2固体在20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1 NH4Cl溶液中的Ksp小
D.在Mg(OH)2的悬浊液中加入NaF溶液后, Mg(OH)2不可能转化为MgF2
查看答案和解析>>
科目:高中化学 来源: 题型:
判断同分异构体的种类(不考虑立体异构):
 (1)某烷烃的相对分子质量为114,且分子中含有两个相同的支链,则该烷烃可能的结构共有 种;
(1)某烷烃的相对分子质量为114,且分子中含有两个相同的支链,则该烷烃可能的结构共有 种;
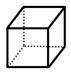
(2)“立方烷”(如图)与氯气发生取代反应,生成的二氯代物共有______种;
(3)甲苯的二氯取代物共有______种;
(4)“金刚烷”(如图),它可看作是由四个等同的六元环组成的空间构型。
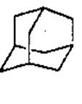 请判断:
请判断:
①一溴代物有 种;
②由氯原子 取代金刚烷亚甲基(-CH2-)中氢原子所形的二氯取代物共有______种。
取代金刚烷亚甲基(-CH2-)中氢原子所形的二氯取代物共有______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
向200ml 0.1mol/L的FeCl2溶液中加入适量的NaOH溶液,使Fe2+恰好完全沉淀,过滤,小心加热沉淀,直到水分蒸干,再灼烧到质量不再变化,此时固体的质量为( )
A.1.14g B.1.6g C.2.82g D.4.36g
查看答案和解析>>
科目:高中化学 来源: 题型:
第三代混合动力车,可以用电动机、内燃机或二者结合推动车辆。汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态。
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,生成1 mol水蒸气放热569.1 kJ。则该反应的热化学方程式为____________________________________________________________。
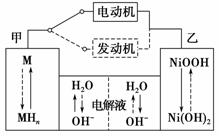
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液。镍氢电池充放电原理示意如图,其总反应式为H2+2NiOOH 2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH________(填“增大”、“减小”或“不变”),该电极的电极反应式为__________________________。
2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH________(填“增大”、“减小”或“不变”),该电极的电极反应式为__________________________。
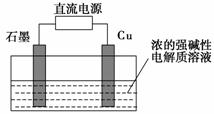
(3)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的______________腐蚀。为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,利用_____________保护法。或与像铅酸蓄电池这样的直流电源的____________(填“正”或“负”)极相连。利用_____________保护法防止其被腐蚀。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com