
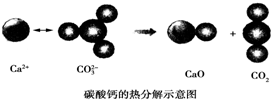
| A. | CO2(g)和CaO(s)的总能量大于CaCO3(s)的总能量 | |
| B. | 由该反应可推出凡是需要加热才发生的反应均为吸热反应 | |
| C. | 该反应的焓变大于零 | |
| D. | 该反应中有离子键断裂也有共价键断裂,化学键断裂吸收能量,化学键生成放出能量 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | CO2、HC1、H2O | B. | HC1、H2O、O2 | C. | HC1、H2O | D. | CO2、O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
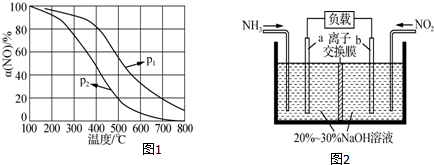
| A. | 在常温下氮气比氧气和氯气稳定 | |
| B. | 氮、氧和氯的单质常温下为气体 | |
| C. | 氮、氧和氯分子在反应过程中释放能量 | |
| D. | 氮气、氧气和氯气的密度不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiH4的沸点高于CH4,推测HCl的沸点高于HF | |
| B. | Fe与CuSO4溶液反应置换出Cu,故Na也能从CuSO4溶液中置换出Cu | |
| C. | 电解熔融NaCl制取Na,故电解熔融MgCl2也能制取Mg | |
| D. | CO2和Na2O2反应生成Na2CO3和O2,故SO2和Na2O2反应生成Na2SO3和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 组成元素相同,各元素质量分数也相同的不同物质属于同系物 | |
| B. | 分子式相同的不同物质一定是同分异构体 | |
| C. | 相对分子质量相同的不同物质一定是同分异构体 | |
| D. | 通式相同的不同物质一定属于同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中国科学家屠呦呦成功提取出青蒿素用于治疗疟疾,挽救许人的生命 | |
| B. | 法国的让彼埃尔索瓦等三位科学家成功研制出分子机器 | |
| C. | 美国的三位科学家在拓扑相变领域的突出贡献 | |
| D. | 中国科学家蔡启瑞院士非酶催化剂合成氨以及化学方面突碳一出贡献 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com