
【题目】有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下。
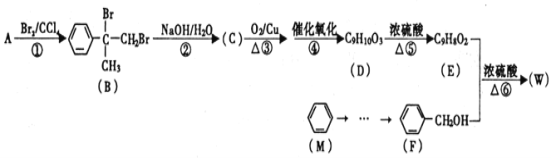
请回答下列问题:
(1)F的化学名称是________,⑤的反应类型是________。
(2)E中含有的官能团是________(写名称),D聚合生成高分子化合物的结构简式为________。
(3)将反应③得到的产物与O2在催化剂、加热的条件下反应可得D,写出反应④的化学方程式________。
(4)④、⑤两步能否颠倒?________(填“能”或“否”)理由是________。
(5)与A具有含有相同官能团的芳香化合物的同分异构体还有________种(不含立体异构),其中核磁共振氢谱为六组峰,且峰面积之比为1:1:2:2:2:2的结构简式为________。
(6)参照有机物W的上述合成路线,以N(分子式为C8H8且属于A的同系物)为原料制备 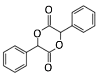 的合成路线(无机试剂任选)_________。
的合成路线(无机试剂任选)_________。
【答案】苯甲醇 消去反应 碳碳双键和羧基 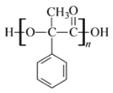
 否 引入碳碳双键,则在醛基被催化氧化的同时,碳碳双键也能被氧化 5
否 引入碳碳双键,则在醛基被催化氧化的同时,碳碳双键也能被氧化 5 ![]()
![]()
【解析】
A→B发生加成反应,则由B的结构可知A为![]() ,A与溴发生加成反应生成B.B发生水解反应生成C为
,A与溴发生加成反应生成B.B发生水解反应生成C为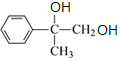 ,C催化氧化的产物继续氧化生成D,则D为
,C催化氧化的产物继续氧化生成D,则D为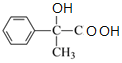 ,对比D、E分子式可知D分子内脱去1分子水生成E,故D在浓硫酸、加热条件下发生消去反应生成E,则E为
,对比D、E分子式可知D分子内脱去1分子水生成E,故D在浓硫酸、加热条件下发生消去反应生成E,则E为![]() ,E与F发生酯化反应生成W为
,E与F发生酯化反应生成W为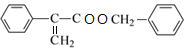 。
。
(1)F 的结构简式为![]() ,则化学名称是苯甲醇;反应⑤是
,则化学名称是苯甲醇;反应⑤是 在浓硫酸的催化作用下发生消去反应生成
在浓硫酸的催化作用下发生消去反应生成![]() ;
;
(2)E的结构简式为![]() ,含有的官能团是碳碳双键和羧基,D为
,含有的官能团是碳碳双键和羧基,D为 ,发生聚合生成高分子化合物的结构简式为
,发生聚合生成高分子化合物的结构简式为 ;
;
(3)C为 ,催化氧化的产物为
,催化氧化的产物为 ,
, 继续氧化生成
继续氧化生成 的反应方程式为
的反应方程式为 ;
;
(4)反应④是催化氧化,而反应⑤是消去,如果颠倒,先引入碳碳双键,则在醛基被催化氧化的同时,碳碳双键也能被氧化,故④、⑤两步不能颠倒;
(5)A的结构简式为![]() ,含有苯环和碳碳双键,其具有含有相同官能团的芳香化合物的同分异构体可能是:①苯环连接甲基和-CH=CH2,共有邻、间和对位三种结构;②苯环只有一个取代基,可能是-CH2CH=CH2或-CH=CHCH3,共2种,则满足条件的同分异构体共5种,其中核磁共振氢谱为六组峰,且峰面积之比为1:1:2:2:2:2的结构简式为
,含有苯环和碳碳双键,其具有含有相同官能团的芳香化合物的同分异构体可能是:①苯环连接甲基和-CH=CH2,共有邻、间和对位三种结构;②苯环只有一个取代基,可能是-CH2CH=CH2或-CH=CHCH3,共2种,则满足条件的同分异构体共5种,其中核磁共振氢谱为六组峰,且峰面积之比为1:1:2:2:2:2的结构简式为![]() ;
;
(6)分子式为C8H8且属于A的同系物,则N为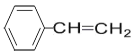 ,
,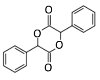 的水解产物为
的水解产物为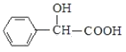 ,而
,而 先与Br2发生加成反应,再水解得到
先与Br2发生加成反应,再水解得到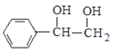 ,
, 连续催化氧化后得到
连续催化氧化后得到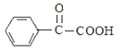 ,而
,而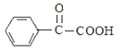 再与H2发生加成反应即可得到
再与H2发生加成反应即可得到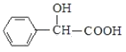 ,则以
,则以 为原料制备
为原料制备  的合成路线为
的合成路线为![]() 。
。


科目:高中化学 来源: 题型:
【题目】铅及其化合物用途广泛,三盐基硫酸铅(3PbO·PbSO4·H2O,摩尔质量=990 g/mol)简称三盐。以铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如图所示。

已知:![]() 。
。
请回答下列问题:
(1)步骤①中涉及的主要反应的平衡常数K=____(列出计算式即可)。步骤②中滤渣的主要成分是____。
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是____(任答一条)。
(3)步骤⑥合成三盐的化学方程式为____。现用100 t铅泥可制得纯净干燥的三盐49.5 t,若铅元素的利用率为75%,则铅泥中铅元素的质量分数为___ %。简述步骤⑦检验沉淀洗涤完全的方法___ 。
(4)已知水中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-,其中Pb(OH)2是沉淀,各形态铅的物质的量的分数α随溶液pH变化的关系如图所示,除去污水中的铅,最好控制溶液的pH在____左右,当溶液的pH由13转化为14时发生反应的离子方程式是:________________

(5)将PbO粗品溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,进一步电解Na2PbCl4生成Pb,如图所示。阴极电极反应式是_________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Zn(s)+1/2O2(g)=ZnO(s) △H=-350.5kJ·mol-1
Hg(l)+1/2O2(g)=HgO(s) △H=-90.8kJ·mol-1
则反应Zn(s)+HgO(s)=ZnO(s)+Hg(l)的△H为( )
A. +519.4kJ·mol-1B. +259.7 kJ·mol-1
C. -259.7 kJ·mol-1D. -519.4kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe3O4中含有Fe2+、Fe3+,分别表示为 Fe(Ⅱ)、Fe(Ⅲ),以Fe3O4/Pd为催化材料,可实现用 H2消除酸性废水中的致癌物 NO2-,其反应过程示意图如图所示,下列说法不正确的是
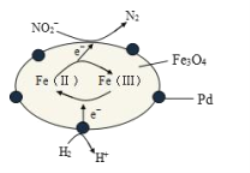
A.用该法处理后水体的 pH降低
B.Fe(Ⅱ)与 Fe(Ⅲ)的相互转化起到了传递电子的作用
C.反应过程中NO2-被 Fe(Ⅱ)还原为 N2
D.Pd 上发生的电极反应为:H2- 2e-== 2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于敞口容器中的反应:Zn(s)+H2SO4(aq)= ZnSO4 (aq)+H2(g),下列叙述中不正确的是
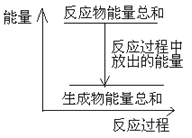
A. Zn和H2SO4的总能量大于 ZnSO4和H2的总能量
B. 反应过程中能量关系可用上图表示
C. 若将该反应设计成原电池,则Zn为负极
D. 若将该反应设计成原电池,当有65g锌溶解时,正极放出11.2L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知镁能分别与O2、N2、CO2反应,反应的化学方程式分别是 2Mg+O2![]() 2MgO、3Mg+N2
2MgO、3Mg+N2![]() Mg3N2、2Mg+CO2
Mg3N2、2Mg+CO2![]() 2MgO+C。把等质量的金属镁分别放在:①足量纯氧气中;②足量二氧化碳气体中;③足量空气中,完全燃烧后,得到的固体物质的质量分别对应的是W1g、W2g和W3g。以下三者的关系正确的是( )
2MgO+C。把等质量的金属镁分别放在:①足量纯氧气中;②足量二氧化碳气体中;③足量空气中,完全燃烧后,得到的固体物质的质量分别对应的是W1g、W2g和W3g。以下三者的关系正确的是( )
A.W1>W2>W3B.W3=W1>W2C.W3>W2>W1D.W2>W1>W3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的1/10。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式。
正极:____________;负极:________。
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用下图所示甲的方案,其中焊接在铁闸门的固体材料R可以采用___。
A、铜 B、钠 C、锌 D、石墨
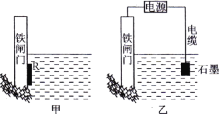
(3)上图中乙方案也可降低铁闸门腐蚀速率,其中铁闸门应该连接在直流电源的________极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中充入NO2,发生反应2NO2(g)![]() N2O4(g)。其它条件相同时,不同温度下平衡体系中各物质的物质的量分数如下表:(已知:N2O4为无色气体)
N2O4(g)。其它条件相同时,不同温度下平衡体系中各物质的物质的量分数如下表:(已知:N2O4为无色气体)
t/℃ | 27 | 35 | 49 | 70 |
NO2% | 20 | 25 | 40 | 66 |
N2O4% | 80 | 75 | 60 | 34 |
下列说法不正确的是( )
A.27℃,该平衡体系中的NO2转化率为![]()
B.平衡时,NO2的消耗速率为N2O4消耗速率的2 倍
C.室温时,将盛有NO2的密闭玻璃球放入冰水中其颜色会变浅
D.其他条件不变,增大NO2起始量,平衡正移,该反应的化学平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列描述正确的是
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B.40gNaOH溶解在1L水中,所制得的溶液,物质的量浓度为1molL﹣1
C.标准状况下,11.2L四氯化碳所含分子数为0.5NA
D.常温常压下,5.6g铁与过量的盐酸反应转移电子总数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com