
 �±���ʵ�߱�ʾĿǰԪ�����ڱ��߸����ڵIJ��ֱ߽磮 �١������Ԫ�������ڱ��е����λ�����£�
�±���ʵ�߱�ʾĿǰԪ�����ڱ��߸����ڵIJ��ֱ߽磮 �١������Ԫ�������ڱ��е����λ�����£�
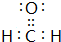 ��
������ ��Ԫ�������ڱ���λ�ã���֪��ΪH����ΪNa����ΪC����ΪN����ΪO����ΪP����ΪS����ΪCl��
��1���ӵ������ڵ�������������Ԫ���У�������������������Ϊ����Ԫ�أ�������������������Ϊ�ǽ����ԣ�
��2��ͬ����������ҷǽ�������ǿ��ͬ�������϶��·ǽ����Լ������ǽ�����Խǿ���⻯��Խ�ȶ���
��3����Ԫ�� �١��ۡ�����ɵĹ��ۻ���������Է���������С��ΪHCHO��
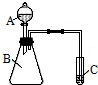
��4�����õ��ʵ���û���Ӧ��֤����������ˮ��Ӧ��������������������
�������������ﷴӦ�û�������֤��������������Һ����β����������
��5��Ԫ�� �ܵ�����������ˮ����XΪHNO3������������ӣ�
��X�����Ԫ����ͬ�����ӻ������X�������ӣ���ˮ��ҺҲ�����ԣ��û�����ΪNH4NO3����Һ��笠�����ˮ������ԣ�
M��Ԫ�� �ܺ� ����ɵ�˫ԭ��������ӣ���MΪNO��ȫ����ˮ���ճ�ΪԪ�آܵ�����������ˮ����HNO3��������Ӧ��4NO+3O2+2H2O=4HNO3�����ݷ���ʽ���㣮
��� �⣺��Ԫ�������ڱ���λ�ã���֪��ΪH����ΪNa����ΪC����ΪN����ΪO����ΪP����ΪS����ΪCl��
��1���ӵ������ڵ�������������Ԫ���У�������������������Ϊ����Ԫ�أ�������������������Ϊ�ǽ����ԣ���ʵ�����ӵ������ڵ��������ڽ����ͷǽ����Ľ�����Ϊ�� ��
��
�ʴ�Ϊ�� ��
��
��2��ͬ����������ҷǽ�������ǿ��ͬ�������϶��·ǽ����Լ������ǽ�����Խǿ���⻯��Խ�ȶ������⻯���ȶ��ԣ�H2O��H2S��PH3��
�ʴ�Ϊ��H2O��H2S��PH3��
��3����Ԫ�� �١��ۡ�����ɵĹ��ۻ���������Է���������С��ΪHCHO������ʽΪ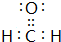 ��
��
�ʴ�Ϊ��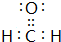 ��
��
��4�����õ��ʵ���û���Ӧ��֤����������ˮ��Ӧ����������������������Ӧ����ʽΪ��2Na+2H2O=2NaOH+H2����
�������������ﷴӦ�û�������֤��C�з�Ӧ�����ӷ���ʽΪS2-+Cl2=2Cl-+S����������������Һ����β����������������C���Թܿڴ���һ��պ������������Һ��������β����
�ʴ�Ϊ��2Na+2H2O=2NaOH+H2����S2-+Cl2=2Cl-+S�����������ƣ�
��5��Ԫ�� �ܵ�����������ˮ����XΪHNO3�����뷽��ʽΪ��HNO3=H++NO3-��
��X�����Ԫ����ͬ�����ӻ������X�������ӣ���ˮ��ҺҲ�����ԣ��û�����ΪNH4NO3�����������ǿ����ʣ���ˮ����ȫ���룬����NH4+ˮ���ʹ��Һ�����ԣ�
M��Ԫ�� �ܺ� ����ɵ�˫ԭ��������ӣ���MΪNO��8.96L NO���ʵ���Ϊ$\frac{8.96L}{22.4L/mol}$=0.4mol��ȫ����ˮ���ճ�ΪԪ�آܵ�����������ˮ����HNO3��������Ӧ��4NO+3O2+2H2O=4HNO3����Ҫ�������ʵ���Ϊ0.3mol������Ҫ��������Ϊ��0.3��6.02��1023��
�ʴ�Ϊ��HNO3=H++NO3-�����������ǿ����ʣ���ˮ����ȫ���룬����NH4+ˮ���ʹ��Һ�����ԣ�0.3��6.02��1023��
���� ���⿼��Ԫ�����ڱ���Ԫ���������ۺ����ã�ע������Ԫ�ػ��������ʣ����ս����ԡ��ǽ�����ǿ���Ƚ�ʵ����ʵ���ǶԻ���֪ʶ���ۺϿ��飮


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ${\;}_{94}^{238}$X��${\;}_{94}^{240}$Y��Ϊͬ�������� | |
| B�� | ${\;}_{94}^{238}$X��${\;}_{92}^{238}$Z��Ϊͬ�������� | |
| C�� | ${\;}_{94}^{240}$Y��${\;}_{92}^{238}$Z������ͬ������ | |
| D�� | ${\;}_{94}^{238}$X��${\;}_{92}^{238}$Z������ͬ��ѧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��0.10mol/L CH3COONa��Һ��ͨ��HCl��c��Na+����c��CH3COOH��=c��Cl-�� | |
| B�� | ��0.10mol/LNaHSO3��Һ��ͨ��NH3��c��Na+����c��NH4+����c��SO32-�� | |
| C�� | ��0.10mol/L Na2SO3��Һͨ��SO2��c��Na+��=2[c��SO32-��+c��HSO3-��+c��H2SO3��] | |
| D�� | ��0.10mol/L�� NH4��2CO3��Һ��ͨ��CO2��c��NH4+��=c��HCO3-��+c��CO32-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 A��B��C��D��E����Ԫ�ص�ԭ��������������A��ԭ������������������B�������������Ǵ���������2����D��L�������ԳɶԵ��ӣ�E+�ĺ������������Ӳ㣬�Ҷ�����ȫ��״̬���Իش�����ͬ�⣮
A��B��C��D��E����Ԫ�ص�ԭ��������������A��ԭ������������������B�������������Ǵ���������2����D��L�������ԳɶԵ��ӣ�E+�ĺ������������Ӳ㣬�Ҷ�����ȫ��״̬���Իش�����ͬ�⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
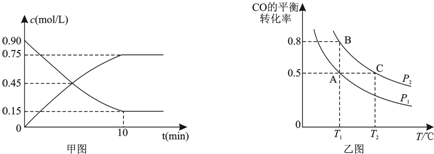
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʵ��ʱ��������ƿ�з��뼸����ʯ�������Ƭ�� | |
| B�� | �������Ż�ʱʹ����ĭ�������� | |
| C�� | ���Թܼ���̼�����ƹ���ʱʹ�Թܿ���������б | |
| D�� | Ũ���ὦ��Ƥ����������ϡ����������Һ��ϴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

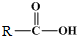 +
+ $\stackrel{����}{��}$
$\stackrel{����}{��}$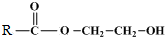
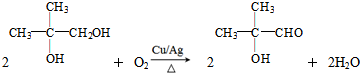 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| 20�� | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
| s��g/100gˮ�� | 111 | 33.7 | 11.1 | 6.34 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com