
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu | B. | Cu2O | C. | CuS | D. | Cu2S |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
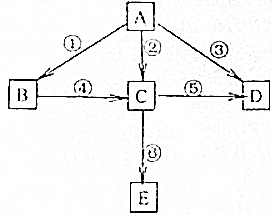 己知A为单质,B、C、D、E为化合物.它们之间存在如图转化关系:
己知A为单质,B、C、D、E为化合物.它们之间存在如图转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂化可获得乙烯、丙烯和丁二烯 | |
| B. | 水玻璃可用于生产黏合剂和防火剂 | |
| C. | 盐析可提纯蛋白质并保持其生理活性 | |
| D. | 二氧化硅是生产光纤制品的基本原料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com