
实验室制得1mL乙酸乙酯后,沿器壁加入0.5mL紫色石蕊试液,这时石蕊试液将存在于饱和碳酸钠层与乙酸乙酯层之间(整个过程不振荡试管)。对可能出现的现象,下列叙述正确的是( )
A.液体分两层,石蕊层仍呈紫色,有机层呈无色
B.石蕊层为三层环,由上而下呈红、紫、蓝色
C.石蕊层有两层,上层呈紫色,下层呈蓝色
D. 石蕊层为三层环,由上而下呈蓝、紫、红色
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
航天器中常使用可充电电池,构造示意图如右图(氢化物电极为储氢金属,可看做H2直接参加反应)。白天太阳能帆板发电,将一部分电量储存在镍氢电池里,夜晚镍氢电池供电。下列说法正确的是( )
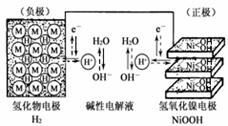
A.在使用过程中此电池要不断补充水
B.放电时NiOOH在电极上发生氧化反应
C.充电时阴极区电解质溶液pH升高
D.充电时阴极反应为Ni(OH)2-e-+OH-= NiOOH+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在特定溶液中一定能大量共存的是
A.pH=12的澄清的溶液中:K+、Na+、MnO4-、SO42-
B.c(Al3+) =0.1 mol·L-1的溶液中:Na+、Cl-、HCO3-、SO42-
C.甲基橙呈红色的溶液中:NH4+、Ba2+、AlO2-、Cl-
D.加入少量铝粉后能产生氢气的溶液中:NH4+、Fe2+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F、G七种元素的原子序数依次递增。已知:
①G的原子序数为29,其余的均为短周期主族元素;
②A是宇宙中含量最多的元素,B原子最外层电子数是次外层电子数的2倍,C原子核外有三个未成对电子;
③D和E原子价电子排布式均为ns2np4;④F的单质是黄绿色气体。
请回答下列问题:
(1)G2+的核外电子排布式是 。在[G(NH3)4]2+离子中,G2+与NH3分子形成的是 键。
(2)与B、C形成的阴离子(BC—)互为等电子体的微粒有 、 (分子和离子各写一种)。
(3)B与C形成的化合物中,下列判断正确的是 。
a.氢化物稳定性:B>C b.氢化物沸点:B<C
c.最高价氧化物的水化物酸性:B<C d.非金属性:B>C
(4)B、C、D第一电离能由小到大的顺序为 (用元素符号作答),B的一种氢化物相对分子质量为26,分子中的σ键与π键数目比为 。
(5)七种元素中,电负性最大的元素与B元素形成化合物电子式为 ,该物质的晶体属于 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组性质比较中,正确的是( )
①酸性:HClO4>HBrO4>HIO4 ②离子还原性:S2->Cl->Br ->I-
③沸点:HF>HCl>HBr>HI ④金属性:K>Na>Mg>Al
⑤气态氢化物稳定性:HF>HCl>H2S ⑥半径:O2->Na+>Na>Cl
A.①②③ B.②③④ C.①④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
煤的气化是煤高效、洁净利用的方向之一。下图为加热某地煤样所得煤气组成及体积分数随温度变化的曲线图。由图可知该煤气中( )
A.只含有碳、氢两种元素
B.所含的有机物是CH4、CnHm、CO
C.CO体积分数小于CH4体积分数
D.氢气体积分数最大
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物蒸汽密度是相同状态下氢气的38倍,现取7.6g该有机物和0.1mol O2在密闭容器中恰好完全反应,生成CO2、CO和H2O。将该混合气体依次通过浓硫酸、灼热的CuO和碱石灰后(假设每一步均充分反应),浓硫酸增重3.6g,CuO固体质量减少1.6g,而碱石灰增重8.8 g。
(1)有机物燃烧的生成物:n(H2O)= mol, n(CO2)= mol。
(2)有机物的分子式为 。
(3)等量的该有机物分别与足量的Na和NaOH反应,消耗Na和NaOH的物质的量之比为2∶1,则该有机物的结构简式为 ,所含官能团的名称为
(4) 在铜作催化剂时,该有机物可被氧气氧化,其反应方程式为
(5)该有机物也能和丁醇(C4H10O)发生酯化反应,在丁醇的同分异构体中,有些能被催化氧化生成醛,写出所有符合上述要求的丁醇的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液与Al反应能放出H2,下列离子在该溶液中一定能大量共存的是 ( )
A.NH4+、Fe2+、Cl-、SO42- B.Na+、K+、Cl-、SO42-
C.Mg2+、H+、Cl-、SO42- D.K+、Ca2+、HCO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
硅基太阳电池需用化合物甲作钝化材料,甲的摩尔质量为140 g·mol-1,其中硅元素的质量分数为60%。已知1 molNH3与足量的化合物乙充分反应后可得到35 g 甲与6 g H2。工业上制乙的流程如下:

请回答下列问题:
(1)乙的电子式是 ;比较热稳定性:乙_______NH3(填>,<或=)。
(2)NH3与足量的化合物乙反应制甲的化学方程式是 。
(3)合成炉内物质需在保护气氛下高温合成,下列气体可作保护气的有 (填字母编号)。
A.O2 B.H2 C.N2 D.CO2 E.Ar
(4)上述生产乙的过程中液氨的作用是_________________________________________。
(5)甲与少量H2SO4溶液反应只得到H2SiO3和盐M两种产物,写出该反应的离子方程式 。请设计验证产物盐M的实验方案
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com