
分析 反应中CO转化为CO2,则n(CO)=n(CO2)=n铁氧化物(O),产生的CO2全部用澄清石灰水吸收,得到沉淀30g为CaCO3,根据碳元素守恒n(CO2)=n(CaCO3),计算Fe的氧化物中Fe元素质量,进而计算Fe原子物质的量确定氧化物化学式.
解答 解:产生的CO2全部用澄清石灰水吸收,得到沉淀30g为CaCO3,根据碳元素守恒n(CO2)=n(CaCO3)=$\frac{30g}{100g/mol}$=0.3mol,反应中CO转化为CO2,则n铁氧化物(O)=n(CO)=n(CO2)=0.3mol,故Fe的氧化物中Fe元素质量=16g-0.3mol×16g/mol=11.2g,故Fe原子物质的量为$\frac{11.2g}{56g/mol}$=0.2mol,则氧化物中Fe、O原子数目之比为0.2mol:0.3mol=2:3,故该铁的氧化物为Fe2O3,
答:该铁的氧化物为Fe2O3.
点评 本题考查化学方程式有关计算,明确反应过程是解题关键,注意利用守恒法进行解答,难度中等.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:解答题
| 配料表 | 精制海盐、碘酸钾[ |
| 含碘量 | 20~40mg/kg |
| 卫生许可证号 | ××卫碘字(1999)第001号 |
| 分装日期 | 见封底 |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X分子中最多可有9个碳原子共平面 | |
| B. | X可以发生取代、加成、聚合等反应 | |
| C. | 1 mol X与足量NaHCO3溶液反应所得物质的分子式为C9H7O4Na | |
| D. | 苯环上的取代基与X完全相同的X的同分异构体有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某离子第三层上和第二层上的电子数均为第一层的4倍 | |
| B. | Cl-的结构示意图: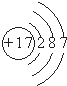 | |
| C. | 某物质的焰色反应为黄色,某物质一定为钠的化合物 | |
| D. | 14C和14N的质量数相等,互称为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe的质量为2.7g,Al的质量为2.8g | B. | Fe的质量为2.8g,Al的质量为2.7g | ||
| C. | Fe的质量为5.4g,Al的质量为5.6g | D. | Fe的质量为5.6g,Al的质量为5.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
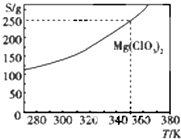 Mg(ClO3)2在农业上可用做脱叶剂、催熟剂.可采用复分解反应制备:MgCl2+2NaClO3═Mg(ClO3)2+2NaCl.已知Mg(ClO3)2的溶解度(S)随温度(T)的变化曲线如图所示.下列有关叙述中不正确的是( )
Mg(ClO3)2在农业上可用做脱叶剂、催熟剂.可采用复分解反应制备:MgCl2+2NaClO3═Mg(ClO3)2+2NaCl.已知Mg(ClO3)2的溶解度(S)随温度(T)的变化曲线如图所示.下列有关叙述中不正确的是( )| A. | 温度越高,Mg(ClO3)2饱和溶液的物质的量浓度越大 | |
| B. | 温度越高,Mg(ClO3)2饱和溶液的质量分数越大 | |
| C. | 350K时,Mg(ClO3)2饱和溶液的物质的量浓度为$\frac{250g}{191g/mol×1L}$ | |
| D. | 350 K时,Mg(ClO3)2饱和溶液的质量分数为$\frac{250g}{350g}$×100% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Sn2+、Fe2+、Ge3+ | B. | Sn2+、Ge3+、Fe2+ | C. | Ge3+、Fe2+、Sn2+ | D. | Fe2+、Sn2+、Ge3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com