
���� ��1������Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�ȡ��ٷֺ������䣬�Լ��ɴ�������һЩ��Ҳ�������仯��
��2������Ũ�ȡ������¶ȡ�����ѹǿ��ʹ�ô���������Ӧ��ĽӴ�����ܼӿ췴Ӧ���ʣ�
��3��ת����Ϊת��������ʼ���ı�ֵ��ת����������������ȣ�������������ת������ȣ�����ʼ���������Ҳ�����ȣ�
��4�����ѻ�ѧ�������������γɻ�ѧ���ų����������n molN2�μӷ�Ӧ�������2molN��N��3nmolH-H�����γ�6nmolN-H�����Դ˼��㷴Ӧ�ȣ�
��5����ѹ�����£���������仯���ﵽƽ��ʱ�����������ܶ��Ƿ�Ӧǰ��1.2���������Ϊԭ����$\frac{1}{1.2}$����ϲ��������㣮
��� �⣺��1��A����Ӧǰ�����������仯������ϵ��ѹǿ���ֲ��䣬��˵���ﵽƽ��״̬����A��ȷ��
B����ʼ���ϱ��Լ�ת���̶�δ֪��ijʱ��H2��NH3��Ũ��֮����3��2������ȷ���Ƿ�ﵽƽ��״̬����B����
C����ͬʱ���ڣ�����6NA��N-H����ͬʱ����3NA��H-H����˵�����淴Ӧ������ȣ��ﵽƽ��״̬����C��ȷ��
D����Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�ijʱ�̷�Ӧ�������㣺3v��N2��=v��H2��������˵���ﵽƽ��״̬����D����
E����������ƽ��Ħ���������䣬��˵����������ʵ������䣬�ﵽƽ��״̬����E��ȷ��
�ʴ�Ϊ��BD��
��2��A�����£���Ӧ������ȣ���A����
B����NH3�������ϵ��Ũ�Ƚ��ͣ���Ӧ���ʼ�С����B����
C�����º��������£�����N2����Ӧ��Ũ������Ӧ��������C��ȷ��
D�����º�ѹ�����£�����He�����������Ũ�ȼ�С����Ӧ���ʼ�С����D����
�ʴ�Ϊ��C��
��3��ת����Ϊת��������ʼ���ı�ֵ��ת����������������ȣ�������������ת������ȣ�����ʼ���������Ҳ�����ȣ�ӦΪ1��3���ʴ�Ϊ��1��3��
��4�����ѻ�ѧ�������������γɻ�ѧ���ų����������n molN2�μӷ�Ӧ�������2molN��N��3nmolH-H�����γ�6nmolN-H������Ӧ�ų�������Ϊn��6c-a-3b��kJ��
�ʴ�Ϊ��n��6c-a-3b����
��5����ѹ�����£���������仯���ﵽƽ��ʱ�����������ܶ��Ƿ�Ӧǰ��1.2���������Ϊԭ����$\frac{1}{1.2}$���跴Ӧǰ���Ϊ1.2L����Ӧ��Ϊ1.0L��
N2����+3 H2��?2 NH3 ��V
1 3 2 2
0.2 1.2-1.0=0.2
�ﵽƽ��ʱ����������а������������Ϊ$\frac{0.2}{1.0}��100%$=20%��
�ʴ�Ϊ��20%��
���� ���⿼���Ϊ�ۺϣ��漰��ѧƽ��ļ��㣬ƽ��״̬���жϡ�ƽ���ƶ���Ӱ�������Լ���Ӧ�ȵļ�������⣬������ѧ���ķ��������ͼ��������Ŀ��飬ע����ռ����˼·�ͽǶȣ��ѶȲ���


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
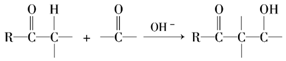 ��
��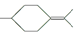 ���������մ��Ľṹ��ʽΪ
���������մ��Ľṹ��ʽΪ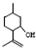 ��
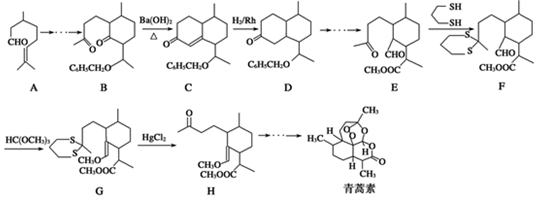
��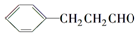 ���ĺϳ�·������ͼ�����Լ���ѡ����
���ĺϳ�·������ͼ�����Լ���ѡ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Һ��ϡ���ᷴӦ��H++OH-=H2O | |
| B�� | ����ϡ���ᷴӦ��2Fe+6H+=2Fe3++3H2�� | |
| C�� | ̼������Һ��ϡ���ᷴӦ��Na2CO3+2H+=2Na++H2O+CO2�� | |
| D�� | ����������Һ��ϡ���ᷴӦ��Ba2++SO42-=BaSO4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ҵ�ϴӷ�Ǧ���ص�Ǧ�����Ǧ�Ĺ����У�����̼������Һ��Ǧ�ࣨ��Ҫ�ɷ�ΪPbSO4��������Ӧ��PbSO4��s��+CO32-��aq��?PbCO3��s��+SO42-��aq����ij��������PbSO4Ϊԭ��ģ��ù��̣�̽��������Ӧ��ʵ���������������ijɷ֣�
��ҵ�ϴӷ�Ǧ���ص�Ǧ�����Ǧ�Ĺ����У�����̼������Һ��Ǧ�ࣨ��Ҫ�ɷ�ΪPbSO4��������Ӧ��PbSO4��s��+CO32-��aq��?PbCO3��s��+SO42-��aq����ij��������PbSO4Ϊԭ��ģ��ù��̣�̽��������Ӧ��ʵ���������������ijɷ֣�| ʵ�鲽�裨��Ҫ��д������������̣� | Ԥ�ڵ�ʵ������ͽ��� |
| ȡһ������Ʒ��ָ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ȼ��仯�������������������й㷺����;���ش��������⣺
�ȼ��仯�������������������й㷺����;���ش��������⣺| ������� | �¶�/�� | �������/L | Cl02��g����ƽ��ת���� |
| a | T1 | V1=l L | 75% |
| b | T1 | v2 | |
| c | T3 | v3 | 75% |
| d | |||
| e |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
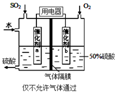 �ش��������⣺
�ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������ɢϵ��ʵ������Ƿ�ɢ�����ӵ�ֱ������1-100 nm֮�� | |
| B�� | �������Һ��һ���Ǿ�һ���ķ�ɢϵ�������ö����ЧӦ������ | |
| C�� | �Ʊ�Fe��OH��3����IJ���Ϊ���ڷ�ˮ����εμ�5��6��FeCl3������Һ�������������Һ�ʺ��ɫ������ֹͣ���� | |
| D�� | �ù��˵ķ������Խ��������Һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
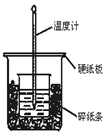 ��֪�Ȼ�ѧ����ʽH+��aq��+OH-��aq���TH2O��l����H=-57.3kJ/mol��
��֪�Ȼ�ѧ����ʽH+��aq��+OH-��aq���TH2O��l����H=-57.3kJ/mol���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Xһ��Ϊ����� | B�� | X����ΪNaCl | ||
| C�� | X���������� | D�� | X�������κλ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com