
 A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题:
A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题:分析 A元素可形成自然界硬度最大的单质,该单质为金刚石,则A为C元素;B与A同周期,核外有三个未成对电子,则B为N元素;根据X原子的第一电离能至第四电离可知,X原子的第四电离能剧增,则X表现+3价,所以X为Al元素;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质,则Y为S元素;Z的一种同位素的质量数为63、中子数为34,则质子数=63-34=29,故Z为Cu元素,据此进行解答.
解答 解:A元素可形成自然界硬度最大的单质,该单质为金刚石,则A为C元素;B与A同周期,核外有三个未成对电子,则B为N元素;根据X原子的第一电离能至第四电离可知,X原子的第四电离能剧增,则X表现+3价,所以X为Al元素;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质,则Y为S元素;Z的一种同位素的质量数为63、中子数为34,则质子数=63-34=29,故Z为Cu元素.
(1)AY2化学式是CS2,其结构式为S=C=S,为直线型结构,属于非极性分子,其分子中每个双键中含有1个σ键,所以CS2分子存在2个σ键,故答案为:非极性;2;
(2)X是Al元素,铝与NaOH溶液反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
XB是CN,晶体与金刚石类似,属于原子晶体;
B的最简单氢化物是NH3,N原子电负性大,分子间形成氢键,所以容易液化,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;原子;分子间形成氢键;
(3)非金属性越强,电负性越强,Al、O、N元素的电负性与非金属性一致,则三种元素电负性大到小顺序为:O>N>Al,故答案为:O>N>Al;
(4)Z为29号Cu元素,根据构造原理,其基态原子核外电子排布式为:1s22s22p63s23p63d104s1;?
①O2中氧元素的化合价是0价,HO2中氧元素的平均化合价是-0.5价,化合价降低作氧化剂,故①正确;?
②HO2为超氧酸,应具有酸性,可与碱反应,故HO2在碱中不能稳定存在,故②正确;
③还原产物是HO2,故③错误;
④1molCu参加反应生成+1价铜离子,有1mol电子发生转移,故④正确,
故答案为:1s22s22p63s23p63d104s1;③;
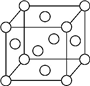
(5)Z为Cu元素,铜原子位于顶点和面心,每个晶胞中含有铜原子的数目为:8×$\frac{1}{8}$+6×$\frac{1}{4}$=4,晶胞中含有4个铜原子,则晶胞的质量为:$\frac{4×64}{{N}_{A}}$g,设该晶胞的边长为xcm,则该晶胞体积为:x3cm3,则::$\frac{64×4}{{N}_{A}}$g=x3cm3×9.00g/cm3,整理可得x=$\root{3}{4.72×1{0}^{-23}}$;
SO42-离子的中心原子S的价层电子对为:4+$\frac{6+2-2×4}{2}$=4,孤电子对数为0,故其空间结构为正四面体,S原子杂化方式为:sp3,
故答案为:$\root{3}{4.72×1{0}^{-23}}$;正四面体;sp3.
点评 本题是对物质结构的考查,涉及核外电子排布、分子结构与性质、杂化方式、晶胞计算等,(5)中晶胞的计算为难点、易错点,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Na在常温下,与空气中的氧气不反应,所以Na不活泼 | |
| B. | Na在空气中燃烧,发出黄色火焰,产物是Na2O | |
| C. | Na是银白色金属,硬度大、熔点高 | |
| D. | Na应保存在煤油中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X有两种常见氧化物,所含的化学键类型完全相同 | |
| B. | N与M形成的化合物的水溶液显酸性 | |
| C. | 离子半径:N>X,Y>M | |
| D. | 气态氢化物的稳定性:Y>M |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醛和乙酸乙酯 | B. | 甲酸和乙酸 | ||
| C. | 甲醛和乙醇 | D. | 甲酸甲酯和乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1:1 | B. | 1:2:1 | C. | 1:3:2 | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com