
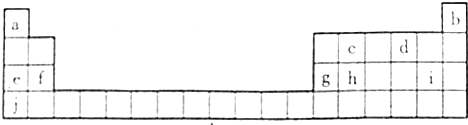
分析 由元素在周期表中的位置可知a、b、c、d、e、f、g、h、i、j分别为H、He、C、O、Na、Mg、Al、Si、Cl、K,
(1)g为Al,位于周期表第ⅢA族,可知最外层电子数;
(2)金属性最强的元素与原子半径最小的元素形成化合物为KH;
(3)制作光导纤维的主要原料为二氧化硅;
(4)设Mg为xmol,Al为ymol,根据质量和生成氢气的体积列方程式计算.
解答 解:由元素在周期表中的位置可知a、b、c、d、e、f、g、h、i、j分别为H、He、C、O、Na、Mg、Al、Si、Cl、K,
(1)g为Al,位于周期表第ⅢA族,最外层电子数为3,故答案为:3;
(2)金属性最强的元素与原子半径最小的元素形成化合物为KH,为离子化合物,电子式为K+[:H]-,故答案为:K+[:H]-;
(3)制作光导纤维的主要原料为二氧化硅,对应元素为Si,故答案为:Si;
(4)设Mg为xmol,Al为ymol,涉及反应有Mg+2H+=Mg2++H2↑、2Al+6H+=2Al3++3H2↑,
则有$\left\{\begin{array}{l}{24x+27y=7.8}\\{x+\frac{3}{2}y=\frac{8.96}{22.4}}\end{array}\right.$,
x=0.1,y=0.2,
n(H2SO4)=n(H2)=$\frac{8.96L}{22.4L/mol}$=0.4mol,
c(H2SO4)=$\frac{0.4mol}{0.8L}$=0.5mol/L,
答:①合金中Mg的物质的量为0.1mol,Al的物质的量为0.2mol;②稀硫酸的物质的量浓度为0.5mol/L.
点评 本题考查位置、结构、性质的关系及应用,为高频考点,把握元素的位置及性质为解答的关键,侧重考查元素化合物性质及化学用语,注重基础知识的夯实,题目难度不大.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:选择题
| A. | 三种溶液中,相关微粒存在如下关系:c(X-)=c(Y-)+c(HY)=c(Z-)+c(HZ) | |
| B. | 三种溶液中离子浓度c(X-)<c(Y-)<c(Z-) | |
| C. | 将三种溶液均加水稀释到1000mL后,三种溶液的pH分别为8、9、10 | |
| D. | HX、HY、HZ的酸性依次增强,电离平衡常数K(HX)>K(HY)>K(HZ) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
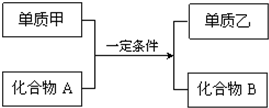 置换反应的通式可表示为:
置换反应的通式可表示为:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
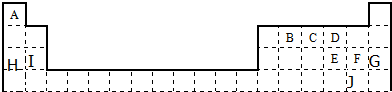
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | ${\;}_{\;}^{37}$Cl2的摩尔质量是74 | |
| B. | 通常情况下,氯气做氧化剂,但氯气也具有还原性 | |
| C. | 35克的${\;}_{\;}^{35}$Cl2含有电子17mol | |
| D. | 常温下,4.48L ${\;}_{\;}^{37}$Cl2含有8NA 个中子(NA 为阿伏加德罗常数) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
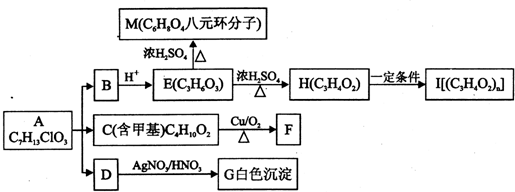
 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$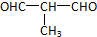 +2H2O.
+2H2O.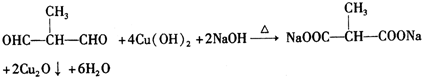 .
.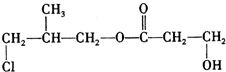
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 ⑥-C6H5 ⑦Br-⑧-COOH ⑨-CH3其中不是官能团的是( )
⑥-C6H5 ⑦Br-⑧-COOH ⑨-CH3其中不是官能团的是( )| A. | ①③④⑥⑧ | B. | ②④⑥⑦⑨ | C. | ②③⑤⑦⑧ | D. | ①③⑤⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com