
Ⅰ.下图是实验室制备乙酸乙酯的装置图,填写下列空白。
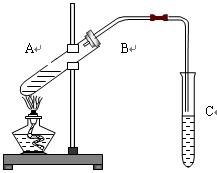
(1)试管A中加入沸石的作用是:__________。导管B的作用是导气和___________。
(2)试管C中的饱和碳酸钠溶液作用是:溶解乙醇、中和乙酸、____________。装置中通蒸汽的导管要插在溶液的液面以上,不能插在溶液中,目的是:________________。
(3)要将乙酸乙酯从试管C的混合物中分离出来,必须用到的仪器是_________。
Ⅱ.下图是实验室石油分馏的装置图,填写下列空白。
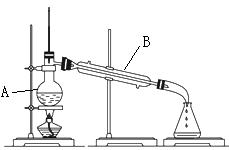
(4)A仪器的名称是____________,B仪器的名称是____________,B仪器内的水流方向是_______________(选答“上进下出”或“下进上出”)。
科目:高中化学 来源: 题型:阅读理解

| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

 TiCl4+2CO
TiCl4+2CO TiCl4+2CO
TiCl4+2CO| 编号 | 装置缺陷和不妥之处 | ① | ② | ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解


| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
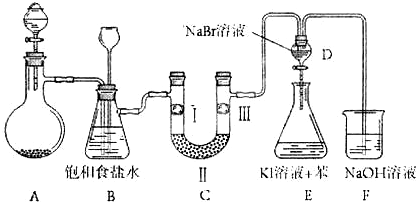
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省德州市高三1月月考化学试卷(解析版) 题型:实验题
熟悉实验仪器,能正确进行实验操作是做好化学实验的前提。
(1)下列有关实验操作或实验事实的叙述,正确的是 (填序号)。
A.实验室中浓硝酸应保存在棕色细口瓶中,并贴有如图所示标签

B.用50mL量筒量取5.6mL浓硫酸
C.中和滴定实验时,锥形瓶洗涤干净并用标准液润洗后,方可注入待测液
D.用四氯化碳萃取碘水中的碘,分液时有机层从分液漏斗的下端放出
E.用广泛pH试纸测得某溶液的pH为4.8
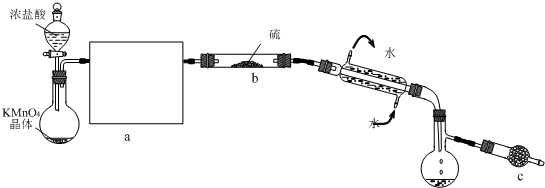
(2)下图是实验室制备氯气并探究氯气是否具有漂白性的实验装置(夹持及加热仪器已省略)。

①A装置中反应的化学方程式为 。
②B装置中仪器a的名称是 。
③B装置的作用是除去气体中混有的HCl,兼起安全瓶的作用,当仪器a中液面不
断上升时,说明 ,此时应停止实验。
④实验中观察到 ,说明干燥氯气无漂白性。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com