
【题目】(1)下面是石蜡油在炽热碎瓷片的作用下产生乙烯并检验其性质的实验,完成下列问题。
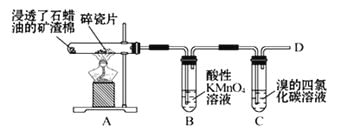
①A中碎瓷片的作用是______________。
②B中反应类型是______________。C中实验现象是__________________________。
③在D处点燃前必须进行的操作是___________________________。
(2)制取氯乙烷(CH3CH2Cl)的最佳方法是(用化学方程式表示):________________。
(3)来自石油的另一产品是苯,请写出由苯制硝基苯的化学方程式:_______________。
(4)该实验中D处乙烯燃烧的化学方程式:_________________________________。
【答案】催化作用 氧化反应 溴的四氯化碳溶液褪色 检验气体的纯度 CH2=CH2+ HCl![]() CH3CH2Cl
CH3CH2Cl ![]() C2H4+ 3O2
C2H4+ 3O2![]() 2CO2+ 2H2O
2CO2+ 2H2O
【解析】
(1)①石蜡油需要在催化剂的作用下才能发生反应,则A中碎瓷片的作用催化作用;
②石蜡油生成的乙烯能被酸性高锰酸钾溶液氧化,反应类型是氧化反应;乙烯含有碳碳双键,能和溴水发生加成反应,C中实验现象是溴的四氯化碳溶液褪色;
③乙烯是可燃性气体,则在D处点燃前必须进行的操作是检验气体的纯度;
(2)制取氯乙烷(CH3CH2Cl)的最佳方法是通过乙烯的加成反应,所以反应的方程式是CH2=CH2+ HCl![]() CH3CH2Cl;
CH3CH2Cl;
(3)在浓硫酸的作用下,苯和浓硝酸发生硝化反应生成硝基苯,反应的化学方程式是![]() ;
;
(4)因此燃烧生成CO2和水,则反应的化学方程式是C2H4+ 3O2![]() 2CO2+ 2H2O。
2CO2+ 2H2O。


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物。
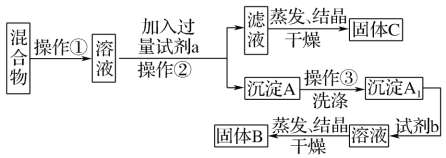
供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸。试回答下列问题:
(1)操作①的名称是____,操作②的名称是____。
(2)试剂a是_____(填化学式,下同),试剂b是____,固体B是____。
(3)加入试剂a所发生反应的化学方程式为_____。加入试剂b所发生反应的离子方程式为_____。
(4)该方案能否达到实验目的:_____(填“能”或“不能”)。若不能,应如何改进?_____(若能,此问不用回答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B![]() 3C+4D反应中,表示该反应速率最快的是( )
3C+4D反应中,表示该反应速率最快的是( )
A.v(A)=0.5mol·L-1·s-1B.v(B)=0.3mol·L-1·s-1
C.v(C)=0.3mol·L-1·s-1D.v(D)=1mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚对苯二甲酸丁二醇酯(PBT)是一种性能优异的热塑性高分子材料。PBT的一种合成路线如图所示:
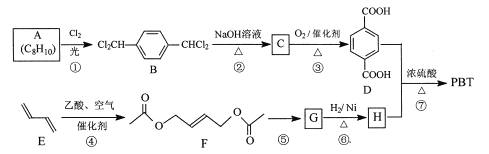
已知:两个羟基同时连在同一碳原子上的结构是不稳定的,它将发生脱水反应: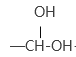 →—CHO
→—CHO
回答下列问题:
(1)A的结构简式为___,C的化学名称为___。
(2)F的分子式为___,⑥的反应类型为___。
(3)⑦的化学方程式是___。
(4)M是H的同分异构体,同时符合下列条件:
a.0.1molM与足量金属钠反应生成氢气2.24L(标准状况)
b.同一个碳原子上不能连接2个羟基
其中核磁共振氢谱显示有3组峰,且峰而积之比为3∶1∶1的结构简式是___。
(5)以2一甲基一1,3一丁二烯为原料(其它试剂任选),设计制备![]() 的合成路线:___。
的合成路线:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4·2H2O)呈淡黄色,可用作晒制蓝图。某实验小组对纯净草酸亚铁晶体热分解气体产物成分的进行探究。小组成员采用如图装置(可重复选用)进行实验:
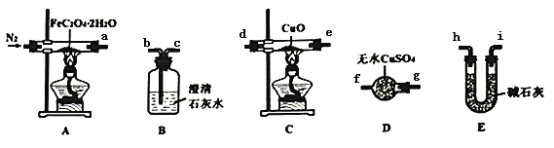
请回答下列问题:
(1)E中盛装碱石灰的仪器名称为___。
(2)D中的现象是___,是为了证明草酸亚铁晶体分解产物中可能含有___。
(3)按照气流从左到右的方向,上述装置的接口顺序为a→g→f→___→尾气处理装置(仪器可重复使用)。
(4)实验前先通入一段时间N2,其目的为___。
(5)实验证明了气体产物中含有CO,依据的实验现象为___。
(6)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A.500℃左右比常温下更有利于合成氨
B.红棕色的NO2,加压后颜色先变深后变浅
C.实验室中常用排饱和食盐水的方法收集氯气
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用硫及其化合物制硫酸有下列三种反应途径,某些反应条件和产物已省略。下列有关说法不正确的是( )
途径①:S![]() H2SO4
H2SO4
途径②:S![]() SO2
SO2![]() SO3
SO3![]() H2SO4
H2SO4
途径③:FeS2![]() SO2
SO2![]() SO3
SO3![]() H2SO4
H2SO4
A. 途径①的反应中体现了浓硝酸的强氧化性
B. 途径②、③的第二步反应在实际生产中可以通过增大氧气的浓度来降低成本
C. 由途径①、②、③分别制取1 mol 硫酸,理论上各消耗1 mol 硫,各转移6 mol 电子
D. 途径②、③比途径①污染相对小且原子利用率高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中只有T为金属元素。
下列判断错误的是
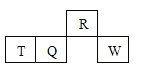
A. 原子半径:T > Q
B. 元素非金属性:Q > R
C. 气态氢化物的热稳定性:R>Q
D. 最高价氧化物对应水化物的酸性: W > Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用王水(浓硝酸和浓盐酸按体积比1:3的混合物)来溶解白金等贵金属进行科学实验。王教授用质量分数为63%的浓硝酸(密度1.40g/ ![]() )和质量分数为36.5%的浓盐酸(密度1.19g/
)和质量分数为36.5%的浓盐酸(密度1.19g/ ![]() )来配制王水600毫升,假设忽略两种酸混合时的体积变化也不考虑混合后的化学变化,下列说法错误的是
)来配制王水600毫升,假设忽略两种酸混合时的体积变化也不考虑混合后的化学变化,下列说法错误的是
A. 该王水中硝酸的物质的量浓度是3.5mol/L
B. 该王水中氧元素的质量是100.8g
C. 该王水的密度约为1.24g/ ![]()
D. 该王水中HCl的质量分数约为26.2%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com