
【题目】粉煤灰中含有SiO2、Al2O3、Fe2O3等,某实验室对其进行处理的流程如图所示:
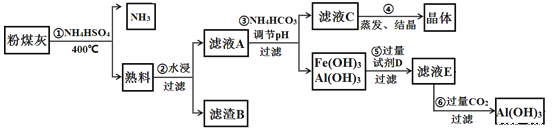
回答下列问题:
(1)第①步得到的“熟料”中可溶性的成分主要是NH4Fe(SO4)2、NH4Al(SO4)2等,写出生成NH4Fe(SO4)2的化学方程式_____________。在NH4Al(SO4)2溶液中加入Ba(OH)2溶液使硫酸根离子恰好完全沉淀,写出反应的离子方程式:____________。
(2)滤渣B的主要成分为_____________。
(3) 已知Ksp[Fe(OH)3]=4×10-38,Ksp [Al(OH)3]=1×10-33。为实现步骤③的实验目的,应使溶液中c(Fe3+)、c(Al3+)均小于或等于1×10-9 molL﹣1可认为完全沉淀,则溶液A至少应调节到pH=_____________。用NH4HCO3调节pH的实验原理为_____________(用离子方程式表示)。
(4)实验室进行第④步操作时,所需的仪器是酒精灯、石棉网、三脚架、__________、_____________。
【答案】(1)Fe2O3+4NH4HSO4![]() 2NH4Fe(SO4)2+2NH3↑+3H2O(2分)
2NH4Fe(SO4)2+2NH3↑+3H2O(2分)
2Ba2++4OH-+NH4++Al3++2SO42-=2BaSO4↓+NH3H2O+Al(OH)3↓(3分)
(2)SiO2(2分)(3)6(3分)H++HCO3-=H2O+CO2↑(2分)
(4)玻璃棒(1分)蒸发皿(1分)
【解析】
试题分析:(1)根据题意,Fe2O3与NH4HSO4反应生成 NH4Fe(SO4)2和氨气与水,反应的化学方程式为Fe2O3+4NH4HSO4![]() 2NH4Fe(SO4)2+2NH3↑+3H2O;在NH4Al(SO4)2溶液中加入Ba(OH)2溶液使硫酸根离子恰好完全沉淀,则还会生成氨水和氢氧化铝沉淀,反应的离子方程式为2Ba2++4OH﹣+NH4++Al3++2SO42﹣=2BaSO4↓+NH3H2O+Al(OH)3↓;
2NH4Fe(SO4)2+2NH3↑+3H2O;在NH4Al(SO4)2溶液中加入Ba(OH)2溶液使硫酸根离子恰好完全沉淀,则还会生成氨水和氢氧化铝沉淀,反应的离子方程式为2Ba2++4OH﹣+NH4++Al3++2SO42﹣=2BaSO4↓+NH3H2O+Al(OH)3↓;
(2)SiO2不溶于一般酸性溶液,不溶于氨水,因此滤渣B的主要成分为SiO2;
(3)根据KSP[Al(OH)3]=1×10﹣33;c(Al3+)均小于或等于1×10﹣9 molL﹣1可认为完全沉淀,c(OH﹣)=![]() mol/L=1×10﹣8mol/L,则常温下溶液的pH=6;在酸性溶液中发生H++HCO3﹣=H2O+CO2↑,所以可以用NH4HCO3调节pH;
mol/L=1×10﹣8mol/L,则常温下溶液的pH=6;在酸性溶液中发生H++HCO3﹣=H2O+CO2↑,所以可以用NH4HCO3调节pH;
(4)实验室进行第④步操作时,滤液C得到硫酸铵,所需的仪器是酒精灯、石棉网、三脚架、玻璃棒、蒸发皿。


科目:高中化学 来源: 题型:
【题目】下列有关元素周期表的说法不正确的是( )
A.第15列某元素能形成碱性气体
B.第2列元素中肯定没有非金属元素
C.第17列的第一种元素的原子序数为8
D.短周期中能与强碱反应产生H2的金属元素位于第ⅢA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a g Mg、Al合金完全溶解在C1 mol·L-1、V1L HCl溶液中,产生bmolH2。再向反应后的溶液中加入C2 mol·L-1、V2 L NaOH溶液,恰好使沉淀达到最大值,且沉淀质量为d g。下列关系错误的是( )
A.![]() B.C1=C2V2/V1
B.C1=C2V2/V1
C.铝为 (12b-a)/9 mol D.与金属反应后剩余盐酸为![]() mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温、常压下X2、Y2、Z2三种气体有如下转化关系:

(1)X2、Y2、Z2分别是 、 、 (填化学式)
(2)Z2与X2Y反应的化学方程式为 .
(3)Z2与NaOH溶液反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组用下图装置进行实验,下列说法正确的是
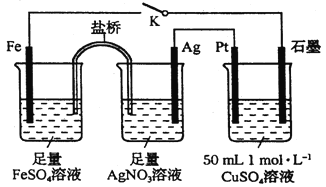
A.盐桥中的电解质可以用KCl
B.闭合K,外电路电流方向为Fe电极→石墨电极
C.闭合K,石墨电极上只生成铜
D.导线中流过0.15mol电子时,加入5.55gCu2(OH)2CO3,CuSO4溶液可恢复原组成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20mL某浓度的AlCl3溶液中滴加2mol/L的NaOH溶液时,所得的沉淀质量与加入NaOH溶液的体积之间的关系如图所示:
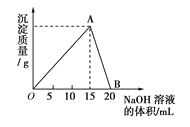
(1)图中A点表示的沉淀是_______,其物质的量是_________;
(2)图中B点溶液中的溶质有______________;
(3)所用AlCl3溶液的物质的量浓度是____________;
(4)当所得沉淀量为0.39g时,用去NaOH溶液的体积是______mL或______mL;
(5)O点到B点反应的总离子方程式为:__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com