
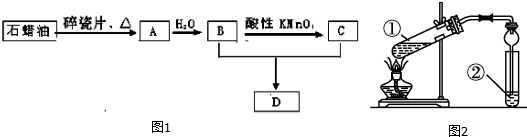
·ÖĪö A²śĮææÉŅŌŗāĮæŅ»øö¹ś¼ŅŹÆÓĶ»Æ¹¤Ė®Ę½µÄøßµĶ£¬ŌņAÓ¦ĪŖCH2=CH2£¬ŹÆĄÆÓĶ·¢ÉśĮŃ»ÆµĆµ½ŅŅĻ©£¬ŅŅĻ©ÓėĖ®·¢Éś¼Ó³É·“Ӧɜ³ÉBĪŖCH3CH2OH£¬ŅŅ“¼±»ĖįŠŌøßĆĢĖį¼ŲŃõ»ÆÉś³ÉCĪŖCH3COOH£¬CH3CH2OHŗĶCH3COOHŌŚÅØĮņĖį×÷ÓĆĻĀ·“Ӧɜ³ÉDĪŖŅŅĖįŅŅõ„£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗA²śĮææÉŅŌŗāĮæŅ»øö¹ś¼ŅŹÆÓĶ»Æ¹¤Ė®Ę½µÄøßµĶ£¬ŌņAÓ¦ĪŖCH2=CH2£¬ŹÆĄÆÓĶ·¢ÉśĮŃ»ÆµĆµ½ŅŅĻ©£¬ŅŅĻ©ÓėĖ®·¢Éś¼Ó³É·“Ӧɜ³ÉBĪŖCH3CH2OH£¬ŅŅ“¼±»ĖįŠŌøßĆĢĖį¼ŲŃõ»ÆÉś³ÉCĪŖCH3COOH£¬CH3CH2OHŗĶCH3COOHŌŚÅØĮņĖį×÷ÓĆĻĀ·“Ӧɜ³ÉDĪŖŅŅĖįŅŅõ„£¬
£Ø1£©øł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬AĪŖCH2=CH2£¬¹Ź“š°øĪŖ£ŗCH2=CH2£»
£Ø2£©·“Ó¦B+C”śDŹĒŅŅ“¼ÓėŅŅĖįŌŚÅØĮņĖį”¢¼ÓČČĢõ¼žĻĀÉś³ÉŅŅĖįŅŅõ„£¬·“Ó¦·½³ĢŹ½ŹĒCH3CH2OH+CH3COOH$”ś_{”÷}^{ÅØĮņĖį}$CH3COOCH2CH3+H2O£¬
¹Ź“š°øĪŖ£ŗCH3CH2OH+CH3COOH$”ś_{”÷}^{ÅØĮņĖį}$CH3COOCH2CH3+H2O£»
£Ø3£©Ź¹1molŅŅĻ©ÓėĀČĘų·¢ÉśĶźČ«¼Ó³É·“Ó¦£¬ĻūŗÄ1molĀČĘų£¬·“Ӧɜ³É1£¬2-¶žĀČŅŅĶé£¬Č»ŗóÓėĀČĘųŌŚ¹āÕÕµÄĢõ¼žĻĀ·¢ÉśĶźČ«Č”“ś·“Ó¦£¬ĻūŗÄ4molĀČĘų£¬ŌņĮ½øö¹ż³ĢÖŠĻūŗÄĀČĘųµÄ×ÜĪļÖŹµÄĮæŹĒ5mol£¬¹Ź“š°øĪŖ£ŗ5£»
£Ø4£©ŹµŃéŹŅÖʱøŅŅĖįŅŅõ„£¬ŹÕ¼Æ²śĪļµÄŹŌ¹ÜÖŠŹ¢·ÅµÄŅŗĢåĪŖ±„ŗĶĢ¼ĖįÄĘČÜŅŗ£¬øĆČÜŅŗæÉŅŌ³żČ„²śĪļÖŠµÄŅŅĖįŗĶŅŅ“¼£¬½µµĶŅŅĖįŅŅõ„ŌŚĖ®ÖŠµÄČܽā¶Č£¬±ćÓŚČÜŅŗ·Ö²ć£¬×°ÖĆÖŠ³¤¾±Ā©¶·³żĘšĄäÄż×÷ÓĆĶā£¬ĮķŅ»ÖŲŅŖ×÷ÓĆŹĒ·ĄÖ¹µ¹Īü£¬
¹Ź“š°øĪŖ£ŗ±„ŗĶĢ¼ĖįÄĘČÜŅŗ£»·ĄÖ¹µ¹Īü£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļĶʶĻ”¢ŅŅĖįŅŅõ„µÄÖʱøµČ£¬ÄŃ¶Č²»“ó£¬×¢Ņāøł¾ŻBĮ¬ŠųŃõ»ÆÉś³ÉŅŅĖį½ųŠŠĶʶĻ£¬²ąÖŲ¶Ō»ł“”ÖŖŹ¶µÄ¹®¹Ģ£®


 Ķ¬²½Į·Ļ°ŗÓÄĻ“óѧ³ö°ęÉēĻµĮŠ“š°ø
Ķ¬²½Į·Ļ°ŗÓÄĻ“óѧ³ö°ęÉēĻµĮŠ“š°ø Ķ¬²½Į·Ļ°Ī÷ÄĻŹ¦·¶“óѧ³ö°ęÉēĻµĮŠ“š°ø
Ķ¬²½Į·Ļ°Ī÷ÄĻŹ¦·¶“óѧ³ö°ęÉēĻµĮŠ“š°ø ²¹³äĻ°Ģā½ĖÕĻµĮŠ“š°ø
²¹³äĻ°Ģā½ĖÕĻµĮŠ“š°ø ѧĮ·æģ³µµĄæŚĖćŠÄĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
ѧĮ·æģ³µµĄæŚĖćŠÄĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓ±±Ź”øßČżÉĻµŚ¶ž“ĪÄ£Äā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
×ī½üÖŠĆĄŃŠ¾æČĖŌ±·¢Ć÷ĮĖŅ»ÖÖæÉæģĖŁ³ä·ÅµēµÄĀĮĄė×Óµē³Ų£¬øƵē³Ųµē½āÖŹĪŖĄė×ÓŅŗĢå{AlCl3/[EMIM]Cl}£¬·ÅµēŹ±ÓŠ¹ŲĄė×Ó×Ŗ»ÆČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ· µÄŹĒ£Ø £©
µÄŹĒ£Ø £©
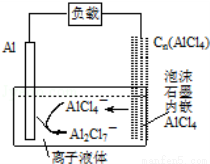
A£®·ÅµēŹ±£¬øŗ¼«·¢Éś£ŗ2AlCl4©©e©=Al2Cl7©+Cl©
B£®·ÅµēŹ±£¬µēĀ·ÖŠĆæĮ÷¹ż3molµē×Ó£¬Õż¼«¼õÉŁ27g
C£®³äµēŹ±£¬ÅŻÄŹÆÄ«¼«ÓėĶāµēŌ“µÄøŗ¼«ĻąĮ¬
D£®³äµēŹ±£¬Ņõ¼« ·¢Éś£ŗ4Al2Cl7©+3e©=Al+7A
·¢Éś£ŗ4Al2Cl7©+3e©=Al+7A lCl4©
lCl4©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĖÄ“ØŹ”øßŅ»ÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠČÜŅŗÖŠ,Cl-µÄĪļÖŹµÄĮæÅضČ×ī“óµÄŹĒ( )
A£®1 mL 0.5 mol”¤L-1µÄNaClČÜŅŗ B£®100 mL 0.01 mol”¤L-1µÄMgCl2ČÜŅŗ
C£®100 mL 0.1 mol”¤L-1µÄAlCl3ČÜŅŗ D£®10 mL 1 mol ”¤L-1µÄKClO3ČÜŅŗ
”¤L-1µÄKClO3ČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĖÄ“ØŹ”ø߶žÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØÖŠ“ķĪóµÄŹĒ
A£®øł¾Ż¶Ō½ĒĻß¹ęŌņ£¬īėŗĶĀĮµÄŠŌÖŹ¾ßÓŠĻąĖĘŠŌ
B£®ŌŚH3O+”¢NH4+ ŗĶ[Cu£ØNH3£©4]2+ÖŠ¶¼“ęŌŚÅäĪ»¼ü
C£®ŌŖĖŲµēøŗŠŌŌ½“óµÄŌ×Ó£¬ĪüŅż¼üŗĻµē×ÓµÄÄÜĮ¦Ō½Ēæ
D£®P4ŗĶCH4¶¼ŹĒÕżĖÄĆęĢå·Ö×ÓĒŅ¼ü½Ē¶¼ĪŖ109o28Ø@
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C4H10 | B£® | C3H8 | C£® | CH4 | D£® | C2H4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 |  |  |  |
| Ķ¼¢ń¼īŠŌŠæĆĢµē³Ų | Ķ¼¢ņĒ¦ĮņĖįŠīµē³Ų | Ķ¼¢óµē½ā¾«Į¶Ķ | Ķ¼¢ōŅųŠæŦæŪµē³Ų |
| A£® | Ķ¼¢ńĖłŹ¾×°ÖĆÖŠ£¬MnO2ŹĒÕż¼«£¬¹¤×÷Ź±Ę仹Ō²śĪļŹĒMnOOH | |
| B£® | Ķ¼¢ņĖłŹ¾×°ÖĆ³äµē¹ż³ĢÖŠ£¬Ņõ¼«µÄµē¼«·“Ó¦Ź½ĪŖPbSO4£Øs£©+2e-=Pb£Øs£©+SO42-£Øaq£© | |
| C£® | Ķ¼¢óĖłŹ¾×°ÖĆ¹¤×÷¹ż³ĢÖŠ£¬µē½āÖŹČÜŅŗÖŠCu2+ ÅØ¶ČŹ¼ÖÕ²»±ä | |
| D£® | Ķ¼¢ōĖłŹ¾µē³ŲÖŠ£¬¹¤×÷Ź±OH-ŅĘĻņŠæµē¼« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com