
120 ℃、101 kPa下,a mL由CO和CH4组成的混合气体在b mL O2中完全燃烧后,恢复到原温度和压强。
(1)若混合气体与O2恰好完全反应,产生b mL CO2,则混合气体中CH4的体积分数为______(保留2位小数)。
(2)若燃烧后气体体积缩小了![]() mL,则a与b关系的数学表达式为_________。
mL,则a与b关系的数学表达式为_________。
(1)0.33 (2)b≥![]()
设混合气体中CO的体积为x,CH4的体积为y,则
2CO + O2====2CO2
x ![]() x
x
CH4 + 2O2![]() CO2+2H2O
CO2+2H2O
y 2y y
则有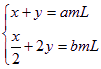
解得y=![]()
所以CH4的体积分数为:![]() ×100%,由于a mL混合气体产生b mL CO2,根据碳原子守恒,则a=b,y=
×100%,由于a mL混合气体产生b mL CO2,根据碳原子守恒,则a=b,y=![]() =
=![]() ,
,
即CH4的体积分数为0.33。
由燃烧反应方程式可知,在120 ℃、101 kPa条件下,CH4燃烧前后体积不变,若燃烧后体积缩小,是由CO燃烧引起的,设CO体积为x′,CH4体积为y′。则:
2CO + O2====2CO2 ΔV
2 1 2 1
x′ ![]() x′
x′ ![]()
CH4 + 2O2![]() CO2+2H2O
CO2+2H2O
y′ 2y′
则有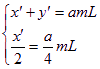
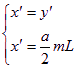
若保证气体完全燃烧,O2必须过量,即b≥(![]() +2y′)。
+2y′)。
即b≥(![]() +a)=
+a)=![]()


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:

| ||
| ||
| ||
| ||
| 25×4 |
| (361.5×10-101×)3NA |
| 25×4 |
| (361.5×10-101×)3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 7a+b |
| 2 |
| 7a+b |
| 2 |
| V1 |
| V2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| a |
| 2 |
| a |
| 2 |
| a |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是___________。
(2)已经在101 kPa时,CO的燃烧热为283 kJ/mol。相同条件下,若2 mol CH4完全燃烧生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是_____________________________________________________。
(3)120°C、101 kPa下,a mL由CO、CH4组成的混合气体在b mL O2中完全燃烧后,恢复到原温度和压强。
①若混合气体与O2恰好完全反应,产生 b mL CO2,则混合气体中CH4的积分数为___________________________(保留2位小数)。
②若燃烧后气体体积缩小了![]() mL,则a与b关系的数学表示式是_________________。
mL,则a与b关系的数学表示式是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com