
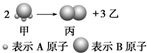
 如图所示:已知甲、乙、丙常温下都为气体.2mol甲分子反应生成1mol丙和3mol乙,
如图所示:已知甲、乙、丙常温下都为气体.2mol甲分子反应生成1mol丙和3mol乙,分析 已知甲、乙、丙常温下都为气体.2mol甲分子反应生成1mol丙和3mol乙,根据结构模型可设甲的分子式为AB3,丙为A2,则乙为B2,混合气体对氢气的相对密度为d,则生成物的相对分子质量为2d,结合质量守恒可知甲的摩尔质量,结合c=$\frac{n}{V}$计算.
解答 解:(1)已知甲、乙、丙常温下都为气体.2mol甲分子反应生成1mol丙和3mol乙,根据结构模型可设甲的分子式为AB3,丙为A2,则乙为B2,
故答案为:B2;
(2)混合气体对氢气的相对密度为d,则生成物的相对分子质量为2d,2mol甲可生成1mol丙和3mol乙,则可知甲的摩尔质量为4d g•mol-1,
故答案为:4d g•mol-1;
(3)甲的物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,质量为0.5mol×4d g•mol-1=2d g,500mL水的质量为500g,则溶液的质量为(500+2d)g,
溶液的体积为$\frac{500+2d}{ρ}×1{0}^{-3}$L,
则物质的量浓度为$\frac{0.5mol}{\frac{500+2d}{ρ}×1{0}^{-3}L}$=$\frac{500ρ}{(2d+500)}$mol/L,
故答案为:$\frac{500ρ}{(2d+500)}$.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的计算能力的考查,本题注意把握物质的构成特点,为本题考查的侧重点,难度不大.


科目:高中化学 来源: 题型:选择题
 ,其命名正确的是( )
,其命名正确的是( )| A. | 2-甲基-4-乙基-4-戊烯 | B. | 2-异丁基-1-丁烯 | ||
| C. | 4-甲基-2-乙基-1-戊烯 | D. | 2,4-二甲基-3-己烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下的22.4L辛烷完全燃烧,生成二氧化碳分子数为8NA | |
| B. | 1mol甲烷的质量与NA个甲烷分子的质量相等 | |
| C. | 28g氮气含有的原子数目为NA | |
| D. | 1mol碳正离子CH5+所含的电子总数为11NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去CO2中混有的CO:用浓NaOH溶液洗气 | |
| B. | 除去BaCO3固体中混有的BaSO4:加过量稀盐酸后,过滤、洗涤 | |
| C. | 除去KNO3溶液中混有的NaCl:蒸发结晶 | |
| D. | 除去Cu粉中混有的CuO:加适量稀硫酸后,过滤、洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上可通过电解熔融的AlCl3来得到金属铝 | |
| B. | 电解饱和食盐水制氯气可采用铁作为阳极 | |
| C. | 炒菜铁锅易生锈是因为形成了原电池,铁作负极 | |
| D. | 工业上一般采用铝热法冶炼金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4L任何气体的物质的量均为1mol | |
| B. | 非标准状况下,1mol任何气体不可能占有22.4L体积 | |
| C. | 0.3molO2、0.3molN2和0.4molCO2组成的混合气体,在标准状况下的体积约为22.4L | |
| D. | 标准状况下,1molCO和1molCO2的体积比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com