
 A、B、C、D均是前四周期元素组成的单质或化合物,它们之间有如下列转化关系:
A、B、C、D均是前四周期元素组成的单质或化合物,它们之间有如下列转化关系:
| ||
| ||


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
| A、某弱酸的酸式盐NaHA溶液中一定有:c(OH-)+2c(A2-)=c(H+)+c(H2A) |
| B、0.1mol?L-1CH3COONa溶液与0.05mol?L-1盐酸等体积混合后的酸性溶液中:c(CH3COO-)>c(CH3COOH)>c(Cl-)>c(H+) |
| C、物质的量浓度相等的HCN溶液和NaCN溶液等体积混合后的溶液中:c(CN-)+2c(OH-)=2c(H+)+c(HCN) |
| D、0.1mol?L-1(NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3?H2O)+c(Fe2+)=0.3mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

 )和阿司匹林有相似的结构,它的一种制备方法如下
)和阿司匹林有相似的结构,它的一种制备方法如下
 与足量的氢溴酸在加热条件下反应的化学方程式为
与足量的氢溴酸在加热条件下反应的化学方程式为查看答案和解析>>
科目:高中化学 来源: 题型:

 和化合物Ⅵ.
和化合物Ⅵ. 的一种同分异构体经氧化后也能得到上述化合物Ⅰ,该同分异构体的结构简式是
的一种同分异构体经氧化后也能得到上述化合物Ⅰ,该同分异构体的结构简式是查看答案和解析>>
科目:高中化学 来源: 题型:
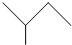
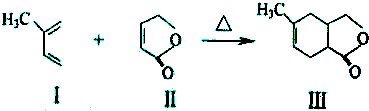
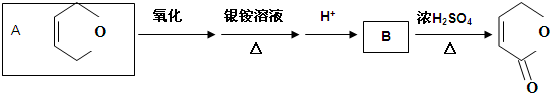
 与CH≡CH(乙炔)也能发生Diels-Alder反应,请写出该反应产物的结构简式
与CH≡CH(乙炔)也能发生Diels-Alder反应,请写出该反应产物的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com