
| A. | HCl、H2SO4中放出H2的速率相同 | |
| B. | CH3COOH中放出H2的速率最快 | |
| C. | H2SO4中放出H2的速率最快,CH3COOH中放出H2的速率最慢 | |
| D. | H2SO4中放出H2的量最多,其余的相等 |
分析 稀盐酸、稀硫酸和醋酸与镁反应都生成氢气,醋酸是弱酸在溶液中部分电离,其氢离子的浓度小于酸的浓度;HCl在溶液中完全电离,其氢离子的浓度等酸的浓度,H2SO4在溶液中完全电离,其氢离子的浓度等于酸的浓度的2倍,
A.放出氢气的速率与氢离子浓度的定性有关;
B.等浓度的三种溶液中,醋酸为弱酸,氢离子浓度最小,放出氢气的速率最小;
C.硫酸溶液中氢离子浓度最大,放出氢气速率最大,醋酸中氢离子浓度最小,放出氢气速率最小;
D.硫酸为二元酸,其氢离子的物质的量最大,盐酸和醋酸都是一元酸,二者能够提供的H的物质的量相等.
解答 解:A.等浓度的盐酸和硫酸溶液中,硫酸溶液中的氢离子浓度大于盐酸,则硫酸放出氢气的速率大,故A错误;
B.醋酸为弱酸,在溶液中只能部分电离出氢离子,则等浓度的三种溶液中,醋酸氢离子浓度最小,放出氢气速率最小,故B错误;
C.硫酸溶液中氢离子浓度最大,与镁反应放出氢气速率最大,醋酸溶液中氢离子浓度最小,与镁反应放出氢气速率最小,故C正确;
D.镁过量,硫酸为二元酸,则其氢离子的浓度等于酸的浓度的2倍,所以硫酸放出的氢气最多,醋酸和盐酸都是一元酸,二者放出氢气的量相等,故D正确;
故选CD.
点评 本题考查了酸和金属的反应、弱电解质的电离,题目难度中等,明确影响酸和足量金属反应生成氢气速率、氢气的量的因素即可解答,试题培养了学生的灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年江西省高二上月考一化学试卷(解析版) 题型:选择题
未来新能源的特点是资源丰富,在使用时对环境无污染或者污染很小,且可以再生。下列属于未来新能源标准的是
①天然气 ②生物质能 ③潮汐能 ④石油 ⑤太阳能 ⑥煤 ⑦风能 ⑧氢能
A.①②③④ B.②③⑤⑦⑧ C.⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯、苯、乙酸分子中的所有原子都在同一平面上 | |
| B. | 蛋白质、淀粉、纤维素和油脂都属于高分子化合物,一定条件下都能水解 | |
| C. | 甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同 | |
| D. | 甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4O | B. | C2H6O | C. | C3H4O2 | D. | C3H6O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用酸性KMnO4溶液除去乙烷中的乙烯 | |
| B. | 乙烷和乙烯都能使酸性KMnO4溶液褪色 | |
| C. | 淀粉、油脂、蔗糖在一定条件下都能发生水解 | |
| D. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
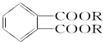 (其中R为烃基),实验室由以下方法可得到DMP:
(其中R为烃基),实验室由以下方法可得到DMP: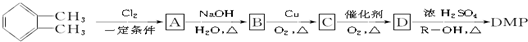
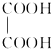 )在一定条件下可以按物质的量1:1发生反应生成高分子化合物,该高分子化合物的结构简式为
)在一定条件下可以按物质的量1:1发生反应生成高分子化合物,该高分子化合物的结构简式为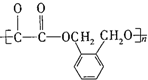 .
.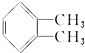 )为原料先生产苯酐(
)为原料先生产苯酐(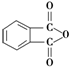 ),再使其与某醇在一定条件下反应制取DMP.苯酐与该醇制取DMP的化学方程式为
),再使其与某醇在一定条件下反应制取DMP.苯酐与该醇制取DMP的化学方程式为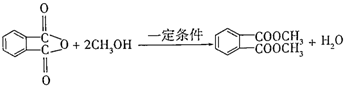 .
.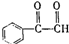 .B也存在多种同分异构体,符合下列条件的B同分异构体有6种.
.B也存在多种同分异构体,符合下列条件的B同分异构体有6种.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com