
【题目】下面合成路线中的化合物I是一种重要的工业原料,用途广泛。

已知:
①烃A的相对分子质量为26。
②化合物B生成化合物C的反应原子利用率100﹪。
③烃E是常用的有机溶剂。
冋答下列问题:
(1)A的化学名称为______________。E分子中共平面的原子数为__________个。
(2)D中的官能团名称是________________。
(3)由B生成C的化学方程式为__________________________。
(4)由E生成F的反应类型为___________;D和H的反应的类型为___________。
(5)同时符合下列条件的G的同分异构体共有____种,任写其中一种的结构简式_____
①能与NaHCO3溶液反应产生气体
②能发生水解反应,且能发生银镜反应
ClCH2COOH是合成甘氨酸的原料之一,现用B物质经两步反应制备ClCH2COOH,合成路线为______________________。(无机试剂任选)
【答案】 乙炔 12 羟基、氨基 2CH2=CH2+O2![]() 2
2![]() 加成反应 取代反应 12 HCOOCH2CH2CH2CH2COOH
加成反应 取代反应 12 HCOOCH2CH2CH2CH2COOH ![]()
【解析】本题考查有机物的合成和推断,(1)烃A的相对分子质量为26,则A的分子式为C2H2,即乙炔,根据F的结构简式,E与氢气反应生成F,此反应是加成反应,即E中含有6个碳原子,也就是3个乙炔分子,通过加成反应,生成E,即E的结构简式为: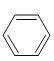 ,根据乙烯是平面结构,因此E中共面的原子是12个;(2)根据D的结构简式,含有官能团是羟基和氨基;(3)B生成C,原子利用率100%,说明只生成一种物质,类似于加成反应,即B的结构简式为CH2=CH2,化学反应方程式为:2CH2=CH2+O2
,根据乙烯是平面结构,因此E中共面的原子是12个;(2)根据D的结构简式,含有官能团是羟基和氨基;(3)B生成C,原子利用率100%,说明只生成一种物质,类似于加成反应,即B的结构简式为CH2=CH2,化学反应方程式为:2CH2=CH2+O2![]() 2
2![]() ;(4)根据(1)的分析,E生成F发生加成反应,D和H生成I,对比它们的结构简式,此反应发生取代反应;(5)①与NaHCO3发生反应,生成CO2,说明含有羧基;②能发生水解反应,且能发生银镜反应,说明是甲酸某酯的形式,存在“
;(4)根据(1)的分析,E生成F发生加成反应,D和H生成I,对比它们的结构简式,此反应发生取代反应;(5)①与NaHCO3发生反应,生成CO2,说明含有羧基;②能发生水解反应,且能发生银镜反应,说明是甲酸某酯的形式,存在“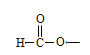 ”,因此有
”,因此有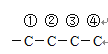 、
、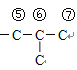 、
、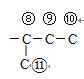 、
、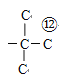 ,羧基的位置有12种,因此符合条件的结构简式有12种,任写一种就行,如HCOOCH2CH2CH2CH2COOH;(6)根据目标产物和原料,先让乙烯引入氯原子和羟基,然后氧化羟基为羧基,
,羧基的位置有12种,因此符合条件的结构简式有12种,任写一种就行,如HCOOCH2CH2CH2CH2COOH;(6)根据目标产物和原料,先让乙烯引入氯原子和羟基,然后氧化羟基为羧基,![]() 。
。


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】某无色溶液可能含有Na+、Ba2+、Al3+、Fe3+、Br-、CO32-等离子,取少量溶液往其中滴加氯水,有无色无味气体产生,溶液仍为无色;另取少量逐滴滴入NaOH 溶液至过量,无现象。关于该溶液的推测正确的是
A. 溶液中可能存在A13+ B. 溶液中可能存在Br-
C. 溶液中一定存在CO32- D. 溶液中可能存在Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一缺电子的粒子结合。如NH4+就是由NH3(氮原子提供电子对)和H+(缺电子)通过配位键形成的。据此,回答下列问题:
(1)下列粒子中可能存在配位键的是________。
A.CO2 B.H3O+ C.CH4 D.H2SO4
(2)硼酸(H3BO3)溶液呈酸性,试写出其电离方程式:___________________。
(3)科学家对H2O2结构的认识经历了较为漫长的过程,最初,科学家提出了种观点:
甲: 、乙:HOOH,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;c.将生成的A与H2反应(已知该反应中H2做还原剂)。
、乙:HOOH,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;c.将生成的A与H2反应(已知该反应中H2做还原剂)。
①如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式)_____________________________________________________________。
②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D四种短周期主族元素,其中原子序数依次增大。已知B和D同主族。A元素的最高正价和最低负价的绝对值之差为2;1molC单质能与冷水反应,在标准状况下生成11.2LH2;D-的电子层结构与Ar原子相同。请回答下列问题:
⑴在下图塔式周期表相应位置标出A、B、C、D四种元素的元素符号。同时在图中将过渡元素涂黑。
 _____________
_____________
⑵用电子式表示B与C形成化合物的过程___________。
⑶图中“钾”和D形成的简单离子的半径大小为________________(用离子符号和“>”、“=”或“<”表示)。
⑷元素非金属性强弱比较有很多方法,其中A和D的非金属性强弱的研究方案中比较可行的是_______(填序号)。
①比较两种单质的颜色②比较氢化物的稳定性
③比较原子半径大小④比较最高价氧化物对应水化物的酸性
⑸A元素能与另外三种元素中的一种元素形成共价化合物,分子中的原子个数比为1:3,相对分子质量为120.5。则该物质的结构式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A、B、C、D各由两种元素组成,甲、乙、丙是短周期元素的三种单质。这些常见的化合物与单质之间存在如下关系(已知C是一种有机物),以下结论不正确的是( )

A. 上图所示的五个转化关系中,有三个是化合反应
B. 上图所示的五个转化关系中,均发生氧化还原反应
C. 常温下,化合物A、B、C、D均为气体
D. 上述转化关系所涉及的化合物中只有一种是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定体积密度为1.32g/cm3的硫酸溶液逐滴滴入到BaCl2溶液中,直到沉淀恰好完全为止。已知反应后所得溶液的质量等于原BaCl2溶液的质量,则原硫酸溶液浓度约为( )
A. 23.9% B. 11.0% C. 13.5mol/L D. 5.67mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如下:

回答下列问题:
(1)A的化学名称为__________。
(2)由C生成D和E生成F的反应类型分别为__________、_________。
(3)E的结构简式为____________。
(4)G为甲苯的同分异构体,由F生成H的化学方程式为___________。
(5)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6∶2∶1∶1,写出2种符合要求的X的结构简式____________。
(6)写出用环戊烷和2-丁炔为原料制备化合物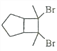 的合成路线________(其他试剂任选)。
的合成路线________(其他试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com