
【题目】A,B,C,D四种物质之间的转化关系如图所示![]() 部分产物已略去
部分产物已略去![]() ,下列说法正确的是
,下列说法正确的是![]()
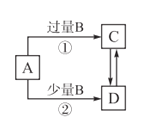
A.若A为![]() 溶液,B可能为氨水,反应
溶液,B可能为氨水,反应![]() 的离子方程式为:
的离子方程式为:![]()
B.若A为Fe,B可能为稀硝酸,反应![]() 的离子方程式为:
的离子方程式为: ![]()
C.若A为NaOH溶液,B可能为![]() ,可用
,可用![]() 溶液鉴别C、D溶液
溶液鉴别C、D溶液
D.若A为![]() ,B可能为
,B可能为![]() ,实验室可用加热固体C的方法制取
,实验室可用加热固体C的方法制取![]()
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
【题目】下列对分子的性质的解释中,不正确的是
A.CH≡C-CH=CH-CH3 中σ键和π键数目之比为 10:3
B.![]() 分子中不含手性碳原子
分子中不含手性碳原子
C.硫难溶于水,微溶于酒精,易溶于 CS2,说明极性:水>酒精>CS2
D.由  知酸性:H3PO4>HClO
知酸性:H3PO4>HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的氨基甲酸置于恒容的密闭真空容器中(固体体积忽略不计),使其达到化学平衡:H2NCOONH4(s)![]() 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表
温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
下列有关叙述正确的是
A. 在低温下该反应能自发进行
B. 15℃时,该反应的化学平衡常数约为2.0
C. 当混合气体平均相对分子质量不变时,该反应达到化学反应限度
D. 恒温条件下,向原平衡体系中再充入2molNH3和1molCO2,达平衡后CO2浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“软电池”采用一张薄层纸片作为传导体,一面镀Zn,另一面镀MnO2。电池总反应为Zn+2MnO2+H2O=2MnO(OH)+ZnO。下列说法正确的是( )
A.该电池的正极为ZnO
B.Zn电极附近溶液的pH不变
C.电池正极的电极反应为2MnO2+2e-+2H2O=2MnO(OH)+2OH-
D.当0.1molZn完全溶解时,流经电解液的电子的物质的量为0.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镀作为一种新兴材料日益被重视,有“超级金属![]() 尖端金属
尖端金属![]() 空间金属”之称。工业上常用绿柱石
空间金属”之称。工业上常用绿柱石![]() 主要成分
主要成分![]() ,还含有铁等杂质
,还含有铁等杂质![]() 冶炼镀,一种简化的工艺流程如下:
冶炼镀,一种简化的工艺流程如下:
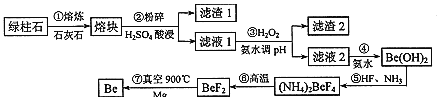
按元素周期表的对角线规则,Be和Al性质相似;几种金属阳离子的氢氧化物沉淀时的pH如表。回答下列问题:
|
|
|
| |
开始沉淀时 |
|
|
|
|
沉淀完全时 |
|
|
|
|
![]() 步骤
步骤![]() 中将熔块粉碎的目的是______;滤渣1的主要成分是_____。
中将熔块粉碎的目的是______;滤渣1的主要成分是_____。
![]() 步骤
步骤![]() 加入
加入![]() 时发生反应的离子方程式为______,从滤液1中得到沉淀的合理pH为______
时发生反应的离子方程式为______,从滤液1中得到沉淀的合理pH为______![]() 填序号
填序号![]() 。
。
A![]() 8
8![]() C
C![]()
![]()
![]() 步骤
步骤![]() 不宜使用NaOH溶液来沉淀
不宜使用NaOH溶液来沉淀![]() 的原因是______。从溶液中得到
的原因是______。从溶液中得到![]() 的实验操作是______、过滤、洗涤、干燥。
的实验操作是______、过滤、洗涤、干燥。
![]() 步骤
步骤![]() 的反应类型是______,步骤
的反应类型是______,步骤![]() 需要隔绝空气的环境,其原因是______。
需要隔绝空气的环境,其原因是______。
![]() 若绿柱石中Be0的含量为
若绿柱石中Be0的含量为![]() ,上述过程生产Be昀产率为
,上述过程生产Be昀产率为![]() ,则1t该绿柱石理论上能生产含镀量
,则1t该绿柱石理论上能生产含镀量![]() 的镀铜台金______t。
的镀铜台金______t。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海底有大量的天然气水合物,可满足人类1000年的能源需要。天然气水合物是一种晶体,晶体中平均每46个水分子构建成8个笼,每个笼可容纳1个CH4分子或1个游离H2O分子。若晶体中每8个笼只有6个容纳了CH4分子,另外2个笼被游离H2O分子填充,则天然气水合物的平均组成可表示为
A.CH4·14H2O
B.CH4·8H2O
C.CH4·![]() H2O
H2O
D.CH4·6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.2mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,下列叙述正确的是( )
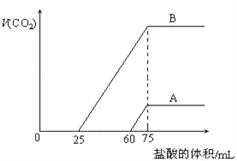
A. A曲线表明原NaOH溶液中通入CO2后,所得溶液中的溶质成分是Na2CO3和NaHCO3
B. B曲线中消耗盐酸0<v(HCl)<25mL时发生的离子反应为:OH-+H+=H2O H++CO32-=HCO3-
C. B曲线表明原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为224mL
D. 原NaOH溶液的物质的量浓度为1.0mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是可逆反应A+2B![]() 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况。由此可推断( )
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况。由此可推断( )
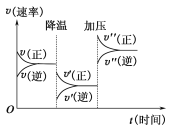
A.温度越高,该反应的化学平衡常数越大B.若A、B是气体,则D是液体或固体
C.逆反应是放热反应D.A、B、C、D均为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从下列事实,不能用勒夏特列原理解释的是 ( )
A. 在溴水中存在如下平衡:Br2+H2O![]() HBr+HBrO当加入NaOH溶液后颜色变浅
HBr+HBrO当加入NaOH溶液后颜色变浅
B. 对![]()
![]()
![]() 平衡体系增加压强使颜色变深
平衡体系增加压强使颜色变深
C. 反应![]()
![]() CO2+NO△H<0升高温度使平衡向逆方向移动
CO2+NO△H<0升高温度使平衡向逆方向移动
D. 合成氨反应:![]()
![]() 2NH3,△H<0 为使氨的产率提高,理论上应采取低温高压的措施
2NH3,△H<0 为使氨的产率提高,理论上应采取低温高压的措施
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com