
����Ŀ��ͭ�����ֳ�����������CuO��Cu2O��ijѧϰС��ȡ0.98 g(�þ�����ƽ����)Cu(OH)2������ȣ���ͭ�����������ɣ����������¶ȱ仯��ͼ1��ʾ�����⣬ijͬѧ������������ʾ����������������������Ԫ�������Ĺ�ϵ���ߣ���ͼ2��ʾ�������з�����ȷ����(����)

A. ͼ1�У�A��B�Ĺ�������0.005 mol���ӷ�����ת��
B. ͼ1���������й�����0.18 gˮ
C. ͼ2���������У���ʾCuO����������CuԪ��������ϵ��������A
D. ͼ1��A��B��ѧʽ�ֱ�ΪCu2O��CuO
���𰸡�B
��������
0.98 g Cu(OH)2���ʵ���Ϊ0.98g��98g/mol=0.01 mol����ȫ������CuO��������Ϊ0.01 mol��80 gmol-1=0.8g������A����CuO����ȫ������Cu2O��������Ϊ0.005 mol��144 gmol-1=0.72g������B����Cu2O��
A.���ݷ�Ӧ����ʽ4CuO![]() 2Cu2O+O2����֪��A��B�Ĺ�����ת�Ƶ������ʵ���Ϊ0.01 mol��A����
2Cu2O+O2����֪��A��B�Ĺ�����ת�Ƶ������ʵ���Ϊ0.01 mol��A����
B.���ݻ�ѧ����ʽCu(OH)2![]() CuO+H2O��4CuO
CuO+H2O��4CuO![]() 2Cu2O+O2����֪��ˮ�����ʵ���Ϊ0.01mol������Ϊ0.01mol��18g/mol=0.18g��B��ȷ��
2Cu2O+O2����֪��ˮ�����ʵ���Ϊ0.01mol������Ϊ0.01mol��18g/mol=0.18g��B��ȷ��
C.10gCuO������CuԪ�ص�����Ϊ��![]() ��64g=8g���۲�ͼ2��֪����ʾCuO����B���ߣ�C����
��64g=8g���۲�ͼ2��֪����ʾCuO����B���ߣ�C����
D.��������������A��B�Ļ�ѧʽ����ΪCuO��Cu2O��D����
��ѡB��


 ��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Na��Mg��Al��0.4mol�ֱ����100mL��2mol/L�������У�ͬ��ͬѹ�²����������������ǣ�
A��1:1:1 B��2:1:1 C��3��1��1 D��1:2:3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʪ����п�ĵ��ѭ����Һ�У��ϸ�Ũ�ȵ�![]() �ḯʴ��������������ܺġ�������Һ��ͬʱ����Cu��CuSO4������CuCl�����Ӷ���ȥ
�ḯʴ��������������ܺġ�������Һ��ͬʱ����Cu��CuSO4������CuCl�����Ӷ���ȥ![]() ��������Һ��ƽ��ʱ�������Ũ�ȵĹ�ϵͼ������˵���������
��������Һ��ƽ��ʱ�������Ũ�ȵĹ�ϵͼ������˵���������
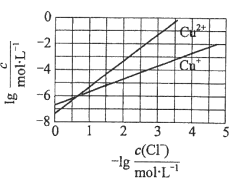
A. ![]() ��������Ϊ
��������Ϊ![]()
B. ��![]() ��ӦΪCu+Cu2++2
��ӦΪCu+Cu2++2![]() =2CuCl
=2CuCl
C. ����CuԽ�࣬Cu+Ũ��Խ�ߣ���![]() Ч��Խ��
Ч��Խ��
D. 2Cu+=Cu2++Cuƽ�ⳣ���ܴ�Ӧ������ȫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��װ�ý���ʵ�飬ʵ��һ��ʱ���������Ԥ�ⲻһ�µ���
�������� | �������� | ʵ��Ԥ�� | |
A | Ũ��ˮ | ��̪��Һ | ������Һ��Ϊ��ɫ |
B | Ũ���� | ����KI��Һ | ������Һ��Ϊ��ɫ |
C | Ũ���� | Ũ��ˮ | ���ձ����а��� |
D | ���͵���������Һ | ϡ��ˮ | ���������Ա仯 |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���ε�طŵ�ʱ�Ļ�ѧ����ʽΪ��2K2S2+KI3=K2S4+3KI���������豸���ӵĵ�·��ͼʾ�����պϿ���Kʱ��X������Һ�ȱ�죮������˵����ȷ���ǣ� ��

A. K+���ҵ���ͨ�����ӽ���Ĥ
B. A�ĵ缫��ӦʽΪ��3I����2e��=I3��
C. ����0.1 mol K+ͨ�����ӽ���Ĥ��X�缫�ϲ�����״��������1.12 L
D. ��س��ʱ��B�缫Ҫ�����Դ�������������缫�Ϸ�����ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ����Ҫ�Ļ���ԭ�ϣ�����ˮ��������ũҩ��������ҩ��ĺϳɵȶ���Ҫ��������
I����ҵ��ͨ�����õ�ⷨ���������۲���ͼ���ش�

(1)��ⷴӦ�Ļ�ѧ����ʽΪ____________________��
(2)����ʳ��ˮͨ���b�˲�����������鷽����____________��
II. ʵ������NaOH��������100 mL 1.0 mol��L-1��NaOH��Һ���Իش����и��⣺
(3)��Ҫ��������ƽ����_______g NaOH���壻
(4)ʵ������������������©�� ��200mL����ƿ ���ձ� �ܲ����� ��ҩ�� ��������ƽ ����������Ҫʵʩ��Һ���ƣ���ȱ�IJ���������___________��________��
(5)����ƿ��ʹ��ǰ������____________��
(6)���ƹ��������²����� �ٳ��� ����Һ ����ȴ ��ϴ�� �ݶ��� ���ܽ� ��ҡ�ȡ�����ȷ�IJ���˳��Ӧ��:�� ��_________��________ ��________ ��________��________�� ��
(7)������������лᵼ��������ҺŨ��ƫ�͵���____________(�����)��
��û��ϴ���ձ��ڱںͲ�����
��δ��ȴ�����¾ͽ���Һת�Ƶ�����ƿ������
����ת�ƹ���������Һ��������
�ܶ���ʱ�۲�Һ��ʱ����
�ݶ��ݺ�����ƿ����ҡ�Ⱥ���Һ����ڿ̶��ߣ���μӼ���ˮ���̶ȴ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѪҺ��Ca2����Ũ��һ�����mg/cm3����ʾ����ȡһ�������Ѫ�����������IJ����[(NH4)2C2O4]��Һ�������������(CaC2O4)���������˲���Ƴ���ϴ�Ӻ�����ǿ��ɵò���(H2C2O4)������KMnO4��Һ�ζ����ɲⶨѪҺ��Ʒ��Ca2����Ũ�ȡ�ij�о���ѧϰС���������ʵ�鲽��ⶨѪҺ��Ʒ��Ca2����Ũ�ȡ�
������KMnO4����Һ����ͼ������50 mL KMnO4����Һ�Ĺ���ʾ��ͼ��


(1)����۲�ͼʾ�жϣ����в���ȷ�IJ�����(�����)________��
(2)����ȷ��50 mL��Һ�����������(������)________��
(3)�����ͼʾ�IJ���������Һ�������Ƶ���ҺŨ�Ƚ�________(�ƫ��ƫС��)��
���ⶨѪҺ��Ʒ��Ca2����Ũ�ȣ���ȡѪ��20.00 mL����������������õ����ᣬ����0.020 mol/L KMnO4��Һ�ζ���ʹ����ת����CO2�ݳ�����ʱ������12.00 mL KMnO4��Һ��
(4)��֪�����KMnO4��Һ��Ӧ�����ӷ���ʽΪ��
2MnO4-��5H2C2O4��6H��===2Mnx����10CO2����8H2O��ʽ�е�x��________��
(5)�������㣬ѪҺ��Ʒ��Ca2����Ũ��Ϊ________mg/cm3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ��������£�����ѡ������ʾ�����ʼ�ת����һ��ʵ�ֵ��ǣ� ��
A.Fe![]() Fe2O3
Fe2O3![]() Fe(OH)3B.Mg(OH)2
Fe(OH)3B.Mg(OH)2![]() MgCl2��Һ
MgCl2��Һ![]() Mg
Mg
C.NH3![]() NO
NO![]() NO2D.SO2
NO2D.SO2![]() (NH4)2SO4
(NH4)2SO4![]() BaSO4
BaSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������һ�ֽྻ������������Դ����������(��Ҫ�ɷ�ΪCO��CO2��)��H2��ϣ����ϳɼ״��������������õķ���֮һ��
(1)������Ӧ�Ĵ�������Cu��Zn��Al��Ԫ�ء�д����̬Znԭ�ӵĺ�������Ų�ʽ��________��
(2)���ݵȵ���ԭ����д��CO���ӵĽṹʽ__________��
(3)�״��������ɵõ���ȩ����ȩ������Cu(OH)2�ļ�����Һ��Ӧ����Cu2O������
�ټ�ȩ������̼ԭ�ӹ�����ӻ�����Ϊ_______________��
�ڼ�ȩ���ӵĿռ乹����___________��1 mol��ȩ��������������ĿΪ______________��
����1��Cu2O����(�ṹ��ͼ��ʾ)�У���������Cuԭ����ĿΪ______________��

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com