
����Ŀ����1����������ʹ��ǰ�������Ƿ�©ˮ����_________(�����)��
A������ƿ B��������ƿ C����Һ©�� D����Ͳ E��������
��2��ʵ������Na2CO3��10H2O��������0.5mol/L��Na2CO3��Һ970mL��Ӧѡ�õ�����ƿ�Ĺ��___________����ȡNa2CO3��10H2O��������_______________��
��3��ijѧ������12mol��L��1Ũ���������ˮ����480mL���ʵ���Ũ��Ϊ0.3 mol��L��1��ϡ���ᡣ
�ٸ�ѧ����Ҫ��ȡ________mL����Ũ����������ơ�
�����ƹ�������ȷ�IJ���˳���ǣ���ĸ��ʾ��ÿ����ĸֻ����һ�Σ�_____��
A. ������ˮϴ���ձ�2��3�Σ�ϴ��Һ��ע������ƿ����
B������Ͳȷ��ȡ����Ũ���ᣬ�ز����������ձ��У��ټ�������ˮ���ò���������������ʹ���Ͼ���
C��������ȴ�������ز�����ע��500mL����ƿ��
D. ������ƿ�ǽ�����ҡ��
E�����ý�ͷ�ιܼ�ˮ��ʹ��Һ����ǡ����̶�����
F������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶�1��2cm��
������ʵ������������Ƶ�ϡ��������ʵ���Ũ���к�Ӱ�죿(���������� ��ƫ�� ��ƫС���� ����Ӱ�족)��
a������Ͳ��ȡŨ����ʱ���ӹ۲찼Һ��_____��
b�����ݺ���ҡ�ȡ����ã�����Һ���½����ټ�����������ˮ_____��
c��ϡ��Ũ����ʱ��δ��ȴ�����¼�ת�Ƶ�����ƿ��_____��
d������ȡŨ�������Ͳ����ϴ�ӣ�����ϴ��Һת�Ƶ�����ƿ��_____��
e������ƿϴ�Ӹɾ���δ����_____��
��4����ͼ��ijͬѧ��ʵ�������Ƹ�NaCl��Һ�Ĺ���ʾ��ͼ�������д������______(��������)��


���𰸡�AC1000mL����ƿ143.012.5BCAFEDƫСƫСƫ��ƫ����Ӱ��٢ۢ�
��������
��1��A������ƿ���в�������ʹ��ǰ�������Ƿ�©ˮ��A��ȷ��
B��������ƿû�в���������ʹ��ǰ���ؼ���Ƿ�©ˮ��B����
C����Һ©�����в�������ʹ��ǰ�������Ƿ�©ˮ��C��ȷ��
D����Ͳû�в���������ʹ��ǰ���ؼ���Ƿ�©ˮ��D����
E��������û�в���������ʹ��ǰ���ؼ���Ƿ�©ˮ��E����
��ѡAC��
��2��ʵ������Na2CO3��10H2O��������0.5mol/L��Na2CO3��Һ970mL������û��970mL������ƿ������Ӧѡ�õ�����ƿ�Ĺ��Ϊ1000mL�����ȡNa2CO3��10H2O��������1L��0.5mol/L��286g/mol��143g��
��3��������480mL���ʵ���Ũ��Ϊ0.3 mol��L��1��ϡ���ᣬӦѡ��500mL����ƿ�������ϡ���������ʵ����ʵ��������֪��ѧ����Ҫ��ȡ����Ũ��������Ϊ500mL��0.3mol��L��1/12 mol��L��1��12.5mL��
����Ũ��������ϡ�����һ�㲽���Ǽ��㡢��ȡ��ϡ�͡���ȴ��ת�ơ�ϴ�ӡ������ݡ�ҡ�ȡ�װƿ�Ȳ�����������ȷ�IJ���˳����BCAFED��
��a������Ͳ��ȡŨ����ʱ���ӹ۲찼Һ�棬ʵ����ȡ��Ũ�����������٣�Ũ��ƫС��
b�����ݺ���ҡ�ȡ����ã�����Һ���½����ټ�����������ˮ����Һ��������ӣ�Ũ��ƫС��
c��ϡ��Ũ����ʱ��δ��ȴ�����¼�ת�Ƶ�����ƿ�У���ȴ����Һ������٣�Ũ��ƫ��
d������ȡŨ�������Ͳ����ϴ�ӣ�����ϴ��Һת�Ƶ�����ƿ�У����ʵ����ʵ������ӣ�Ũ��ƫ��
e������ƿϴ�Ӹɾ���δ�����Ӱ�졣
��4���ܽ��Ȼ��Ʋ�������Ͳ�н��У�Ӧ�����ձ��У��ٴ���ת��ʱ��������ĩ��Ҫ������ƿ�̶��ߵ��·����۴�����ʱӦ����ƽ�ӿ̶��ߣ��ݴ���ѡ�٢ۢݡ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ڹ��������£��������ֽ�����
A. HClO B. KCl C. AgBr D. HNO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������һ����Ҫ�Ļ���ԭ�Ϻͺϳ��м��塣��֪��������,����������ˮ,���¶���28������78��ʱ,���ܽ�ȿ�����20����ijʵ��С��������ɫ������H2O2��������ϩ�ϳɼ�����,��Ӧ���Ʊ�װ�����£�
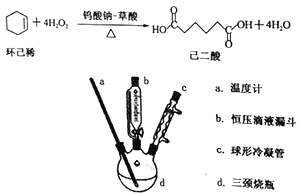
��Ҫʵ�鲽�裺
����100mL������ƿ�����μ���1.50g������0.57g�����34mL30%����������Һ�������´�������20min��
���ú�ѹ��Һ©����������8.0mL�Ļ���ϩ���������貢���Ȼ���2Сʱ��ֹͣ���ȡ�
�۽���ӦҺѸ��ת���ձ��У���ȴ�����º����ñ�ˮԡ��ȴ���д�����������������,����������ˮϴ�ӣ����ɵõ������ᾧ���Ʒ��
�ش��������⣺
(1)��ʵ����ʹ�ô��̶ȵĺ�ѹ��Һ©������Ҫ������_________��_________��
(2)��������ñ�ˮϴ�Ӿ����Ŀ����______________________________________��
�����ᾧ���Ʒ������_________������һ����ô�Ʒ��
(3)ȡ0.1480g������(Mr=146.0)��Ʒ����250mL��ƿ��,����50mL����ˮ�ܽ⣬�ټ���2��ָʾ������0.1000mol/Ld��NaOH����Һ�ζ����յ㣬����NaOH��Һ�����Ϊ20.00mL��
�ٱ�ʵ��Ӧѡ��_________(����ȡ���ʯ���̪��)��Һ��ָʾ����
���жϵζ��յ�ķ�����_________________________��
����Ʒ�м��������������Ϊ_________%(����4λ��Ч����)��
(4)ʵ��С��ͨ���ı价��ϩ��������̽�����ϱȶԲ��ʵ�Ӱ�죬ʵ��������ͼ��ʾ��
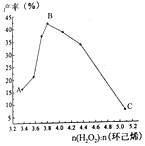
���ͼ��������ʱ仯�Ŀ���ԭ��
��A���B�㣺___________________________________________��
��B���C�㣺____________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£������������Ϊ 1.0L�ĺ����ܱ������з�����Ӧ��2CH3OH(g) CH3OCH3(g) + H2O(g) ����˵����ȷ���ǣ� ��
���� ��� | �¶�(��) | ��ʼ���ʵ���(mol) | ƽ�����ʵ���(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
II | 387 | 0.40 | ||
III | 207 | 0.20 | 0.090 | 0.090 |
A. �÷�Ӧ������ӦΪ���ȷ�Ӧ
B. �ﵽƽ��ʱ������I�е�CH3OH�������������II�е�С
C. ����I�з�Ӧ����ƽ������ʱ�������III�ij�
D. ����ʼʱ������I�г���0.15mol ��CH3OH��0.15mol ��CH3OCH3��0.10mol ��H2O����Ӧ��������Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ļ�����Ӧ�ù㷺������������Ҳ����Ҫ�Ŀ�����Ⱦ��֮һ��Ҫ������д����������á�
I.������:
��1����֪H2��ȼ������H= -285.8kJ/mol��N2(g) +O2(g)=2NO(g) ��H= + 180kJ/mol��һ����������H2��ԭNO����Һ̬ˮ��һ�������ʵ��Ȼ�ѧ����ʽΪ_______________________��
II.���Ϸ�:
��ҵ����NO��Cl2�����Ʊ���Ҫ�ĺϳ����Լ�NOCl( ��������)���塣
��2��NOCl��N Ԫ�صĻ��ϼ�Ϊ__________��NOCl�ĵ���ʽΪ_____________________��
��3����1L��������������ͨ��2molNO(g)��1molCl2(g)������Ӧ:2NO(g) + Cl2(g)![]() 2NOCl(g) ��H���ڲ�ͬ�¶��²��c(NOCl)��ʱ��t�Ĺ�ϵ��ͼ��ʾ��
2NOCl(g) ��H���ڲ�ͬ�¶��²��c(NOCl)��ʱ��t�Ĺ�ϵ��ͼ��ʾ��

�ٸ÷�Ӧ����H_____0(����>"����<������=��)��������_____________________��
���¶�T1ʱ��Cl2(g)��0~20min��ƽ����Ӧ����Ϊ__________mol/(L��min)��
���¶�T2ʱ���÷�Ӧ��ƽ�ⳣ��K=______(�������С�����2λ)������Ӧ��T2�ﵽƽ������������г���2molNO(g)��1molCl2(g)�����ٴ�ƽ��ʱ��c(NOCl)=______(����>������<������һ��)1mol/L��
III.�绯ѧ��:
����ͼ��ʾװ�ÿ���ģ������NO2����̬���ʵĹ��̡�

��4����װ�������缫��ӦʽΪ____________________________��
��5��������������Һ��ͨ������NH3�������̬���ʵIJ�����������____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����б仯ʱ����˷���ͬ�������������ǣ� ��
A.ʯӢ�ɱ����ۻ�B.ʳ�κͱ����ۻ�C.̼�����ƺ�ˮ�ķֽ�D.ʳ�κ��ռ���ۻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ������̫���ܹ���-��ѧ��Ϸֽ������о��л���½�չ�����װ����ͼ��ʾ������˵����ȷ����
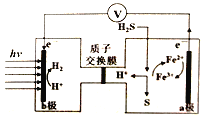
A. ��������й�������ת��Ϊ��ѧ��
B. ��װ�ù���ʱ��H+��b��������a����
C. a���Ϸ����ĵ缫��ӦΪFe3++e-=Fe2+
D. a�����費�ϲ��京Fe3+��Fe2+����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪25��ʱ����HF(aq)+OH-(aq)=F-(aq)+H2O��1����H=-67��7kJ��mol-1��
�� H+(aq)+OH-(aq)=H2O��1�� ��H=-57��3kJ��mol-1����20mL0��1mol��L-1������м���VmL0��1mol��L-1NaOH��Һ�������й�˵������ȷ���ǣ� ��
A. �����ĵ��뷽��ʽ����ЧӦ�ɱ�ʾΪ��HF(aq)![]() F-(aq)+ H+(aq) ��H=-10��4kJ��mol-1
F-(aq)+ H+(aq) ��H=-10��4kJ��mol-1
B. ��V=20ʱ����Һ�У�c(OH-)=c(HF)+c(H+)
C. ��V=20ʱ����Һ�У�c(F-)<c(Na+)=0��1mol��L-1
D. ��V>0ʱ����Һ�п��ܴ��ڣ�c(Na+)>c(F-)>c(OH-)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС�����ʵ���Ʊ�Ca(NO2)2��ʵ��װ����ͼ��ʾ(�г�װ������ȥ)����֪:2NO+CaO2==Ca(NO2)2��2NO2+CaO2==Ca(NO3)2������˵������ȷ����

A. ͨ��N2��Ϊ���ž�װ���еĿ���
B. װ��B��D�е��Լ��ɷֱ�Ϊˮ��Ũ����
C. ��ͭƬ����ľ̿Ҳ�����Ʊ��������������
D. ����װ��A������������Һ��ϡ������Է���CO2��CO
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com