
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÖŠ“ķĪóµÄŹĒ£Ø £©
A.Ąė×Ó¾§ĢåŌŚČŪ»ÆדĢ¬ĻĀÄܵ¼µē
B.ŌŚ¾§ĢåÖŠÖ»ŅŖÓŠŅõĄė×Ó¾ĶŅ»¶ØÓŠŃōĄė×Ó
C.Ō×Ó¾§ĢåÖŠŅ»¶ØÓŠ·Ē¼«ŠŌ¹²¼Ū¼ü
D.·Ö×Ó¾§ĢåÖŠ²»Ņ»¶Øŗ¬ÓŠ¹²¼Ū¼ü
”¾“š°ø”æC
”¾½āĪö”æ
A£®Ąė×Ó¾§ĢåŌŚČŪ»ÆŹ±»į·¢ÉśµēĄė£¬“ęŌŚ×ŌÓÉŅĘ¶ÆµÄĄė×Ó£¬Äܹ»µ¼µē£¬¹ŹAÕżČ·£»
B£®¾§ĢåÖ»ŅŖÓŠŅõĄė×Ó¾ĶŅ»¶ØÓŠŃōĄė×Ó£¬µ«ŗ¬ÓŠŃōĄė×ӵIJ»Ņ»¶ØÓŠŅõĄė×Ó£¬Čē½šŹō¾§Ģ壬¹ŹBÕżČ·£»
C£®Ō×Ó¾§ĢåÖŠ²»Ņ»¶Øŗ¬ÓŠ·Ē¼«ŠŌ¹²¼Ū¼ü£¬Čē¶žŃõ»Æ¹č£¬¹ŹC“ķĪó£»
D£®·Ö×Ó¾§ĢåÖŠæÉÄܲ»ŗ¬»Æѧ¼ü£¬ČēĻ”ÓŠĘųĢ壬¹ŹDÕżČ·£»
¹ŹŃ”C”£


 Ņ»ĻßĆūŹ¦ĢįÓÅŹŌ¾ķĻµĮŠ“š°ø
Ņ»ĻßĆūŹ¦ĢįÓÅŹŌ¾ķĻµĮŠ“š°ø Ńō¹āŹŌ¾ķµ„ŌŖ²āŹŌ¾ķĻµĮŠ“š°ø
Ńō¹āŹŌ¾ķµ„ŌŖ²āŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŖÖ¤Ć÷ijČÜŅŗÖŠ²»ŗ¬ÓŠFe3£«¶ųæÉÄÜŗ¬ÓŠFe2£«£¬½ųŠŠČēĻĀŹµŃé²Ł×÷Ź±×ī¼ŃĖ³ŠņĪŖ( )
¢Ł¼ÓČė×ćĮæĀČĖ®””¢Ś¼ÓČė×ćĮæKMnO4ČÜŅŗ””¢Ū¼ÓČėÉŁĮæKSCNČÜŅŗ
A. ¢Ł¢Ū B. ¢Ś¢Ū
C. ¢Ū¢Ł D. ¢Ł¢Ś¢Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©»łĢ¬Fe2+Ąė×ÓÓŠ______øöĪ“³É¶Ōµē×Ó£¬»łĢ¬NiŌ×ӵĵē×ÓÅŲ¼Ź½ĪŖ__________”£
£Ø2£©ÓĆ”°>”±»ņ”°<”±ĢīæÕ£ŗ
µŚŅ»µēĄėÄÜ | ČŪµć | ĖįŠŌ |
Si_____S | NaCl______Si | H2SO4_____HClO4 |
£Ø3£©F2ĶØČėĻ”NaOHČÜŅŗÖŠæÉÉś³ÉOF2£¬OF2·Ö×Ó¹¹ŠĶĪŖ_______”£ĘäÖŠŃõŌ×ÓµÄŌӻƷ½Ź½ĪŖ_____”£
£Ø4£©ÓėH2O»„ĪŖµČµē×ÓĢåµÄŅ»ÖÖŃōĄė×ÓĪŖ________£ØĢī»ÆѧŹ½£©£»
£Ø5£©NiÄÜÓėCOŠĪ³ÉÕżĖÄĆęĢåŠĪµÄÅäŗĻĪļNi(CO)4,1mol Ni(CO)4ÖŠŗ¬ÓŠ______mol¦Ņ¼ü”£
£Ø6£©CaF2ÄŃČÜÓŚĖ®£¬µ«æÉČÜÓŚŗ¬A13+µÄČÜŅŗÖŠ£¬ŌŅņŹĒ________£ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£©”£ŅŃÖŖAlF63+ČÜŅŗÖŠæÉĪČ¶Ø“ęŌŚ”£
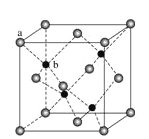
£Ø7£©ZnSŌŚÓ«¹āĢ唢¹āµ¼Ģå²ÄĮĻ”¢ĶæĮĻ”¢ŃÕĮĻµČŠŠŅµÖŠÓ¦ÓĆ¹ć·ŗ”£Į¢·½ZnS¾§Ģå½į¹¹ČēĶ¼ĖłŹ¾£¬Ę侧°ū±ß³¤ĪŖ540.0 pm£¬ĆܶČĪŖ_______£ØĮŠŹ½²¢¼ĘĖć£©£¬aĪ»ÖĆS2-Ąė×ÓÓėbĪ»ÖĆZn2+Ąė×ÓÖ®ĪŹµÄ¾ąĄėĪŖ_____pm£ØĮŠŹ½±ķŹ¾£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬½«20.0gÖŹĮæ·ÖŹżĪŖ14.0%µÄKNO3ČÜŅŗøś30.0gÖŹĮæ·ÖŹżĪŖ24.0%µÄKNO3ČÜŅŗ»ģŗĻ£¬µĆµ½µÄĆܶČĪŖ1.15g”¤cm-3µÄ»ģŗĻČÜŅŗ”£¼ĘĖć£ŗ
£Ø1£©»ģŗĻŗóČÜŅŗµÄÖŹĮæ·ÖŹż___________”£
£Ø2£©»ģŗĻŗóČÜŅŗµÄĪļÖŹµÄĮæÅضČ_____________”£
£Ø3£©ŌŚ1000gĖ®ÖŠŠčČܽā_____________Ħ¶ūKNO3²ÅÄÜŹ¹ĘäÅضČĒ”ŗĆÓėÉĻŹö»ģŗĻŗóČÜŅŗµÄÅضČĻąµČ£æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖĻĀĮŠČČ»Æѧ·½³ĢŹ½£ŗ
¢ŁCH3COOH(l)£«2O2(g)===2CO2(g)£«2H2O(l)””¦¤H1£½£870.3 kJ”¤mol£1
¢ŚC(s)£«O2(g)===CO2(g)””¦¤H2£½£393.5 kJ”¤mol£1
¢ŪH2(g) £«![]() O2(g)===H2O(l)
O2(g)===H2O(l)
¦¤H3£½£285.8 kJ”¤mol£1
Ōņ·“Ó¦2C(s)£«2H2(g)£«O2(g)===CH3COOH(l)µÄ¦¤HĪŖ(””””)
A. £488.3 kJ”¤mol£1 B. £244.15 kJ”¤mol£1
C. 488.3 kJ”¤mol£1 D. 244.15 kJ”¤mol£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķĪŖŌŖĖŲÖÜĘŚ±ķĒ°ĖÄÖÜĘŚµÄŅ»²æ·Ö£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ(””””)

A. Yµ„ÖŹŌŚæÕĘųÖŠČ¼ÉÕÉś³ÉYO3
B. ZŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĖįŠŌ×īĒæ
C. XµÄĒā»ÆĪļĪŖH2X
D. Y”¢ZŗĶWµÄŅõĄė×Ó°ė¾¶ŅĄ“ĪŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ»Æѧ·“Ó¦A2(g)£«B2(g)===2AB(g)µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£¬ÅŠ¶ĻĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ(””””)
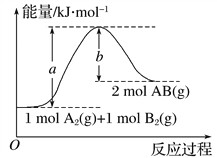
A. ¶ĻĮŃ1 mol A”ŖAŗĶ1 mol B”ŖB¼ü£¬·Å³öa kJÄÜĮæ
B. ĆæÉś³É2 mol AB(g)ĪüŹÕb kJÄÜĮæ
C. øĆ·“Ó¦ÖŠ·“Ó¦ĪļµÄ×ÜÄÜĮæøßÓŚÉś³ÉĪļµÄ×ÜÄÜĮæ
D. øĆ·“Ó¦ČȦ¤H£½(a£b) kJ”¤mol£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬AŹĒæÉÓĆĄ“¶Ō×ŌĄ“Ė®½ųŠŠĻū¶¾µÄ»ĘĀĢÉ«µ„ÖŹĘųĢ壬A”¢B”¢C”¢D”¢E ¶¼ŗ¬XŌŖĖŲ£¬Ęä×Ŗ»Æ¹ŲĻµČēĻĀĶ¼ĖłŹ¾”£
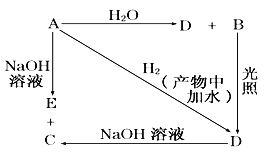
£Ø1£©Ēė·Ö±šŠ“³öA”¢B”¢C”¢D”¢EµÄ»ÆѧŹ½(ČēĪŖČÜŅŗĒėĢīČÜÖŹµÄ»ÆѧŹ½£©£ŗ
A _____£¬B _____£¬C ______£¬D_____£¬E___________”£
£Ø2£©Š“³öĻĀĮŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½:
A+H2O£ŗ______________£»
A+NaOH£ŗ______________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»Æѧ»ī¶ÆæĪÉĻ£¬Čż×éѧɜ·Ö±šÓĆĶ¼Ź¾¼×”¢ŅŅĮ½×°ÖĆ£¬Ģ½¾æ”°NaHCO3ŗĶNa2CO3ÓėĻ”ŃĪĖįµÄ·“Ó¦”±£¬°“±ķÖŠµÄŹŌ¼ĮÓĆĮ棬ŌŚĻąĶ¬Ģõ¼žĻĀ£¬½«Į½øöĘųĒņÖŠµÄ¹ĢĢå·ŪÄ©Ķ¬Ź±µ¹ČėŹŌ¹ÜÖŠ£Ø×°ÖƵÄĘųĆÜŠŌĮ¼ŗĆ£©”£Ēė»Ų“š£ŗ
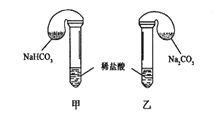
£Ø1£©ø÷×é·“Ó¦æŖŹ¼Ź±£¬____________£Ø¼×”¢ŅŅ£©×°ÖĆÖŠµÄĘųĒņĢå»żĻȱä“ó£¬øĆ×°ÖĆÖŠ·“Ó¦µÄ»Æѧ·“Ó¦·½³ĢŹ½ŹĒ_____________”£
£Ø2£©µ±ŹŌ¹ÜÖŠ²»ŌŁÓŠĘųĢåÉś³ÉŹ±£¬Čż×鏵Ńé³öĻÖ²»Ķ¬ĻÖĻó£¬ŹŌ·ÖĪöŌŅņ²¢ĢīŠ“ĻĀ±ķµÄæÕøń”£
ŹŌ¼ĮÓĆĮæ | ŹµŃéĻÖĻó £ØĘųĒņĢå»ż±ä»Æ£© | ·ÖĪöŌŅņ | |
µŚ¢Ł×é | 0.42gNaHCO3 0.53gNa2CO3 3mL 4mol”¤L-1ŃĪĖį | ¼×ÖŠĘųĒņÓėŅŅÖŠĘųĒņµÄĢå»żĻąµČ | ¼×”¢ŅŅŃĪĖį¾ł¹żĮæ n(NaHCO3)= n(Na2CO3) V¼×(CO2)= VŅŅ(CO2) |
µŚ¢Ś×é | 0.3gNaHCO3 0.3gNa2CO3 3mL 4 mol”¤L-1ŃĪĖį | ¼×ÖŠĘųĒņ±ČŅŅÖŠĘųĒņµÄĢå»ż“ó | A£ŗ___________ |
µŚ¢Ū×é | 0.6gNaHCO3 0.6gNa2CO3 3mL 2 mol”¤L-1ŃĪĖį | ¼×ÖŠĘųĒņ±ČŅŅÖŠĘųĒņµÄĢå»ż“ó | B£ŗ______________ |
ʬæĢŗó£¬ŅŅÖŠĘųĒņÓÖĖõŠ”£¬¼×ÖŠĘųĒņµÄĢå»ż»ł±¾²»±ä | £ØÓĆ»Æѧ·½³ĢŹ½±ķŹ¾£© C£ŗ___________ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com