
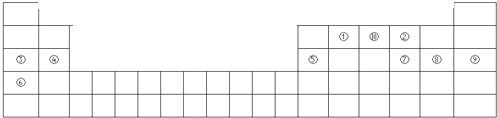
 ���ԭ��صĵ缫���Ϻ͵������Һ����д�������ĵ缫��ӦΪ
���ԭ��صĵ缫���Ϻ͵������Һ����д�������ĵ缫��ӦΪ| ԭ�� | N | S | O | Si |
| �뾶r/10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
 ����������������̼�Ǻ���̼��˫���ķǼ��Է��ӣ�
����������������̼�Ǻ���̼��˫���ķǼ��Է��ӣ� ���Ȼ�þ��þ���Ӻ�������֮��ͨ�����Ӽ��γɵ����ӻ�����õ���ʽ��ʾ����γɹ���Ϊ��
���Ȼ�þ��þ���Ӻ�������֮��ͨ�����Ӽ��γɵ����ӻ�����õ���ʽ��ʾ����γɹ���Ϊ�� ��
�� ��O=C=O��
��O=C=O�� ��
�� ��
�� ���缫��ӦΪ��Al-3e-=Al3+���ʴ�Ϊ��
���缫��ӦΪ��Al-3e-=Al3+���ʴ�Ϊ�� ��Al-3e-=Al3+��
��Al-3e-=Al3+��32 16 |
| 35x+37y |
| x+y |
32 16 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| NaOH(aq) |
| �� |
| CO2 |
| O2��ȼ |
| H2O |
| NH3CO2 |
| �� |
| HCl(aq) |
| �� |
| ʯ���� |
| ȼ�� |
| A���٢ۢ� | B���ڢۢ� |
| C���ڢܢ� | D���٢ܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ڢ�A��Ԫ�صĽ����Աȵڢ�A��Ԫ�صĽ�����ǿ |
| B���ڢ�A��Ԫ�ص��⻯���У��ȶ��Դ��ϵ������μ��� |
| C��ͬ���ڷǽ����������Ӧ��ˮ��������Դ�����������ǿ |
| D����������Ԫ�ص����Ӱ뾶��������С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��
�� ��
��
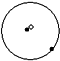
 ��ʾ���ӻ���ӣ�
��ʾ���ӻ���ӣ� ��ʾ���ӣ��������йص�������ȷ���ǣ�������
��ʾ���ӣ��������йص�������ȷ���ǣ�������| A���٢ڢ�Ϊͬ�������� |
| B���٢ڢۻ�Ϊͬλ�� |
| C���٢ڢ������ֻ�ѧ���ʲ�ͬ������ |
| D���٢ڢ۾�����ͬ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ij�¶��£���ͬpH������ʹ�����Һ�ֱ��ˮϡ�ͣ�pH����Һ����仯��������ͼ��ʾ�������ж���ȷ���ǣ�������
ij�¶��£���ͬpH������ʹ�����Һ�ֱ��ˮϡ�ͣ�pH����Һ����仯��������ͼ��ʾ�������ж���ȷ���ǣ�������| A����ͬ���ʱ��c����Һ�кͼ����������a�� |
| B��b����Һ�ĵ����Ա�c����Һ�ĵ�����ǿ |
| C��b�����Ũ�ȴ���a�����Ũ�� |
| D����Ϊ����ϡ��ʱ��pH�仯���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ca��ClO��2��Һ�У�c��Ca2+����c��ClO-����c��OH-����c��H-�� |
| B��������������ʵ���Ũ�ȵ�Na2SO3��Һ��NaHSO3��Һ��ϣ�c��Na+��=c��SO32-��+c��HSO3-��+c��H2SO3�� |
| C����0.2mol��L-1��ijһԪ��HA��Һ��0.1mol��L-1��NaOH��Һ�������Ϻ���Һ��pH����7����Ӧ��Ļ��Һ��2c��OH-��+c��A-��=2c��H+��+c��HA�� |
| D��ij��Һ��ˮ�������c��OH-��=1��10-amol��L-1��a��7ʱ����pH����Һ��һ��Ϊ14-a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| һ������ |
| ŨH2SO4 |
| �� |


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH4 C2H4 |
| B��CH4 C3H6 |
| C��C2H4 C3H4 |
| D��C2H2 C3H4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��c��Na+��=c��CH3COO-�� |
| B��c��CH3COO-��+c��CH3COOH��=0.1 mol?L-1 |
| C����ˮ���������c��OH-��=1.0��10-11 mol?L-1 |
| D��������Һ�м���0.05 mol?L-1��CH3COONa��pHֵ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com