
【题目】在实验室里,使Al2(SO4)3溶液中的Al3+全部沉淀出来,应选用
A. NaCl溶液 B. 氨水 C. 稀硫酸 D. NaOH溶液
科目:高中化学 来源: 题型:
【题目】对K2Cr2O7 + 14HCl (浓) =2KCl + 2CrCl3 +3Cl2↑+7H2O,当0.1molK2Cr2O7反应时,可知
A.1.4mol HCl被氧化 B.转移电子数1.806×1023
C.氧化产物为0.3mol D.还原产物为KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家发现C60分子(图1)由60个碳原子构成,它的形状像足球(图1C),含有C=C键,因此又叫足球烯.1991年科学家又发现一种碳的单质﹣﹣碳纳米管,是由六边环形的碳原子构成的具有很大表面积管状大分子(图1D),图1A、图1B分别是金刚石和石墨的结构示意图.图中小黑点或小黑圈均代表碳原子. 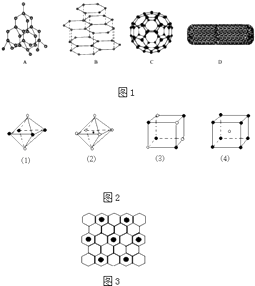
(1)金刚石、石墨、足球烯和碳纳米管四种物质互称为同素异形体,它们在物理性质上存在较大的差异,其原因是;
(2)同条件下,足球烯、石墨分别和气体单质F2反应时,足球烯的化学性质比石墨要活泼,其理由是:;
(3)燃氢汽车之所以尚未大面积推广,除较经济的制氢方法尚未完全解决外,还需解决H2的贮存问题,上述四种碳单质中有可能成为贮氢材料的是:;
(4)图2是从NaCl或CsCl晶体结构图中分割出来的部分结构图,试判断NaCl晶体结构的图象是(填序号);
(5)图1A金刚石结构中一个碳原子被(填数字)个六元环共用;
(6)如图1B,同一层中的原子构成许许多多的正六边形,此单质与熔融的钾单质相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图3所示,该物质的化学式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿原酸被誉为“第七类营养素”,具有广泛的杀菌、消炎功能,其结构简式如图所示.下列有关绿原酸的说法中正确的是( ) 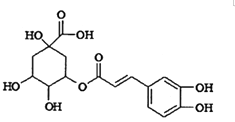
A.绿原酸分子中含有3种官能团
B.1 mol绿原酸最多能与7molNaOH发生反应
C.绿原酸能发生取代反应、加成反应和消去反应
D.绿原酸能使酸性高锰酸钾溶液、浓溴水褪色,但反应原理不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对X+2Y=X2++2Y-的叙述中正确的是( )
A. Y被还原,X2+是还原产物 B. Y被还原,X发生氧化反应
C. X是还原剂,Y被氧化 D. 氧化性:X > Y-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘循环工艺不仅能吸收SO2降低环境污染,同时还能制得氢气,具体流程如下: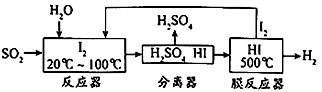
下列说法正确的是( )
A.分离器中的物质分离操作为过滤
B.膜反应器中,增大压强有利于提高HI的分解速率和平衡转化率
C.该工艺中I2和HI的相互转化体现了“碘循环”
D.碘循环工艺的总反应为2SO2+4H2O+I2 = H2+2H2SO4+ 2HI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)有A、B、C、D、E五种短周期主族元素,原子序数由A到E逐渐增大。
①A元素最外层电子数是次外层电子数的2倍。
②B的阴离子和C的阳离子与氖原子的电子层结构相同。
③在通常状况下,B的单质是气体,0.1molB的气体与足量的氢气完全反应共有0.4mol电子转移。
④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体,此淡黄色固体能与AB2反应可生成B的单质。
⑤D的气态氢化物与其最高价含氧酸间能发生氧化还原反应。
请写出:
(1)A元素的最高价氧化物的电子式 。
(2)B元素在周期表中的位置 。
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有 。
(4)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为______________。
(5)C与D能形成2:1的化合物,用电子式表示该化合物的形成过程的 。
(6)元素D与元素E相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 (填选项序号)。
a.常温下D的单质和E的单质状态不同
b.E的氢化物比D的氢化物稳定
c.一定条件下D和E的单质都能与钠反应
d.D的最高价含氧酸酸性弱于E的最高价含氧酸
e.D的单质能与E的氢化物反应生成E单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,在容积为0.5L的密闭容器中发生某一反应,且测得不同时间容器中四种物质A、B、C、D的物质的量变化如图所示. 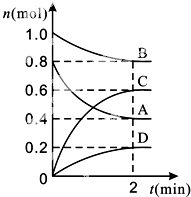
已知:物质A、B、C均为气态、D为固态,正反应是吸热反应.根据要求回答下列问题:
(1)容器中反应的化学方程式为 .
(2)前2min,v(A)=mol(minL)﹣1 .
(3)能说明该反应已达到平衡状态的是 .
A.混合气体的压强不变
B.混合气体的密度不变
C.消耗0.1mol的B同时生成0.1mol的D
D.B的物质的量不变
(4)T℃时,该反应的平衡常数K=(保留小数点后两位). 反应达到平衡后,只增加B的物质的量,则平衡移动方向为;平衡常数K(填增大.减小或不变).
(5)反应达到平衡后,改变下列措施能使A的转化率增大的是 (填选项字母).
A.只增加A的物质的量
B.移走一部分D
C.升高反应体系的温度
D.把容器的体积缩小一倍
(6)T℃时,容积为1L的密闭容器中,起始时充入0.2mol A、0.4mol B、0.3mol C、0.5mol D,此时v(正)v(逆) (填“>”“<”或“=”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com