
���� ���ݳɼ������Ƿ��ʧ���ã���ѧ����Ϊ���Ӽ������ۼ������й��ۼ����б����ԡ������ԣ����ݹ��õ��Ӷ��Ƿ���ƫ�ƣ������ۼ���Ϊ���Լ��뼫�Լ������ݵ����Ƶ��ص���ʽ�����ۼ���Ϊ�Ҽ���м�����A��B��ԭ�Ӽ�ֻ�γ���һ�����ۼ�������������ص���ʽͷ��ͷ����A��B��ԭ�Ӽ����γ�n�����ۼ�ʱ��ֻ��1���Ҽ��������Ϊ�м���
��� �⣺���ݳɼ������Ƿ��ʧ���ã���ѧ����Ϊ���Ӽ������ۼ������й��ۼ����б����ԡ������ԣ�
���ݹ��õ��Ӷ��Ƿ���ƫ�ƣ������ۼ���Ϊ���Լ���Ǽ��Լ������õ��Ӷ�ƫ��Ϊ���Լ������õ��ӶԲ�ƫ�Ƶ�Ϊ�Ǽ��Լ���
���ݵ����Ƶ��ص���ʽ�����ۼ���Ϊ�Ҽ���м����������ԡ�ͷ��ͷ����ʽ�ص���Ϊ�Ҽ����ԡ��粢�硱��ʽ�ص���Ϊ�м���
��A��B��ԭ�Ӽ�ֻ�γ���һ�����ۼ������ڦҼ�������������ص���ʽΪ��ͷ��ͷ������A��B��ԭ�Ӽ����γ�n�����ۼ�ʱ��ֻ��1���Ҽ��������Ϊ�м��������У�n-1�����м���
�ʴ�Ϊ�����Ӽ��빲�ۼ������ۼ������Լ���Ǽ��Լ����Ҽ���м���ͷ��ͷ����n-1����
���� ���⿼�鹲�ۼ���������������ȷ���ۼ������������Ҽ���м��е������ص���ʽ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �ۡ�����Ⱦ������ָ�������� | ��Ҫ ��Ⱦ�� | ���� �����ȼ� | ||
| SO2 | NO2 | PM10 | ||
| 23 | 35 | 56 | PM10 | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
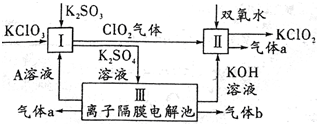 ����أ�KC1O3����������أ�KClO2�������ת����KClO2�ڼ��Ի��������ȶ����ڣ�����KClO2����Ҫ������ͼ��ʾ��
����أ�KC1O3����������أ�KClO2�������ת����KClO2�ڼ��Ի��������ȶ����ڣ�����KClO2����Ҫ������ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڷ�Ӧ���У�����3mol����ת��3mol���� | |
| B�� | �ڷ�Ӧ���У�����������������ǻ�ԭ���� | |
| C�� | �ڷ�Ӧ���У�����11.2L������ת��2mol���� | |
| D�� | �ɷ�Ӧ��֪�����ڿ����м�ǿ�Ȼ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H+��Na+��OH- | B�� | Na+��NO3-��Cl- | ||
| C�� | K+��H+��HCO3- | D�� | Ca2+��SO42-��CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
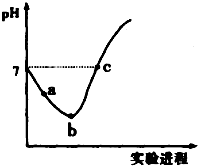 �����£���Cl2����ͨ��ˮ�������ͣ�Ȼ�������ñ�����ˮ�еμ�0.1mol•L-1 ��NaOH ��Һ������ʵ���������Һ��pH �仯������ͼ��ʾ������������ȷ���ǣ�������
�����£���Cl2����ͨ��ˮ�������ͣ�Ȼ�������ñ�����ˮ�еμ�0.1mol•L-1 ��NaOH ��Һ������ʵ���������Һ��pH �仯������ͼ��ʾ������������ȷ���ǣ�������| A�� | ��a ����ʾ��Һ��ͨ��SO2����Һ�����Ժ�Ư���Ծ���ǿ | |
| B�� | b ����ʾ����Һ�У�c��H+����c��Cl-����c��ClO-����c��HClO�� | |
| C�� | ��a �㵽b ��Ĺ����У���Һ��$\frac{c��{H}^{+}��}{c��Cl{O}^{-}��}$ ��С | |
| D�� | c ����ʾ��Һ�У�c��Na+ ��=2c��ClO-��+c��HClO�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com