
【题目】氧化铁和铁粉的混合物19.2 g,恰好溶于150 mL某浓度的稀硫酸,并收集到3.36 L(标准状况下)的气体.向反应后的溶液中滴加硫氰化钾溶液,不显血红色.求:
(1)与稀硫酸反应的铁的物质的量.___________
(2)稀硫酸的物质的量浓度._____________
【答案】0.15 mol 2mol /L
【解析】
根据Fe2O3、Fe的混合物与硫酸恰好完全反应生成了铁的硫酸盐,反应后反应加入KSCN溶液,无血红色出现,说明只生成FeSO4,,发生反应为:Fe+H2SO4=FeSO4+H2↑、Fe+Fe2O3+3H2SO4=3FeSO4+3H2O,根据生成的氢气计算与硫酸反应的Fe的质量,进而计算与硫酸反应的Fe、Fe2O3的质量,再计算混合物中Fe的质量,根据守恒可以知道原硫酸溶液中n(H2SO4)=n(FeSO4),再根据c=n/V计算。
(1)Fe、Fe2O3的混合物与硫酸恰好完全反应,生成了铁的硫酸盐,反应后反应加入KSCN溶液,无血红色出现,说明只生成FeSO4,发生反应为:Fe+H2SO4=FeSO4+H2↑、Fe+Fe2O3+3H2SO4=3FeSO4+3H2O,n(H2)=![]() =0.15mol,则:
=0.15mol,则:
Fe+H2SO4=FeSO4+H2↑
1 1
n(Fe) 0.15mol,
n(Fe)=0.15mol,所以答案为:0.15mol;
(2)根据上述分析可知 m(Fe)=0.15mol![]() 56g/mol=8.4g,故与硫酸反应的Fe2O3和Fe的质量为19.2g-8.4g=10.8g,由Fe+Fe2O3+3H2SO4=3FeSO4+3H2O可知,消耗硫酸的量为0.15mol,生成FeSO4为0.15mol,溶液中总的FeSO4为0.15mol+0.15mol=0.3mol,故根据守恒可以知道原硫酸溶液中n(H2SO4)=n(FeSO4)=0.3mol,原硫酸溶液的物质的量浓度为c =
56g/mol=8.4g,故与硫酸反应的Fe2O3和Fe的质量为19.2g-8.4g=10.8g,由Fe+Fe2O3+3H2SO4=3FeSO4+3H2O可知,消耗硫酸的量为0.15mol,生成FeSO4为0.15mol,溶液中总的FeSO4为0.15mol+0.15mol=0.3mol,故根据守恒可以知道原硫酸溶液中n(H2SO4)=n(FeSO4)=0.3mol,原硫酸溶液的物质的量浓度为c = ![]() =2mol/L;答案:2mol/L。
=2mol/L;答案:2mol/L。


科目:高中化学 来源: 题型:
【题目】有机物M(C6H4S4)是隐形飞机上吸波材料的主要成分。某化学兴趣小组为探究其组成和分子结构,进行如下实验:
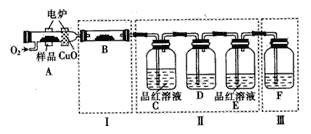
(1)将少量样品放入燃烧管A中,通入足量O2,用电炉加热使其充分燃烧,并将燃烧产物依次通入余下装置(夹持仪器的装置已略去)。
①写出A中样品燃烧的化学方程式______。
②装置B的目的是验证有机物中含氢元素,则B中盛装的试剂可为______。
③D中盛放的试剂是______(填序号)。
a.NaOH溶液b.品红溶液c.KMnO4溶液d.饱和石灰水
④装置A中燃烧管放入CuO的作用是______。
⑤指出装置F的错误______。
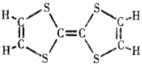
(2)M的结构简式如图所示,4.08g M可使_____mol氢气发生反应,同样质量的M完全燃烧需要消耗氧气_____mL(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某一溴代烷与浓NaOH的醇溶液共热时产生3种沸点不同的消去产物,该一溴代烷至少应含有________个碳原子,其中一种结构简式可表示为____________。
Ⅱ.某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式为________。
(2)A中的碳原子是否都处于同一平面?________(填“是”或者“不是”);
Ⅲ.有机物A分子式为C3H6O2,把它进行实验并记录现象如下:
NaOH溶液 | 银氨溶液 | 新制Cu(OH)2 | 金属钠 | |
A | 发生水解反应 | 有银镜反应 | 有红色沉淀 | 不反应 |
A的结构简式为:_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光刻胶(I)是半导体制造的一种重要材料,其中一种合成路线如下,完成下列填空。
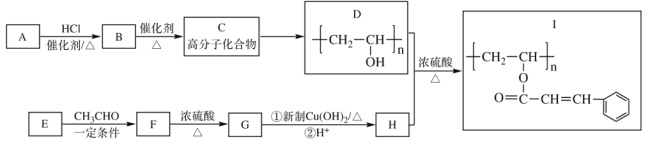
已知:![]()
(1)A的电子式_____________,E的结构简式_____________;
(2)C→D反应的试剂和条件为_____________,F→G的反应类型_____________;
(3)D+H→I的化学反应方程式___________________________________________;
(4)H的芳香类同分异构体中,可以发生水解反应和银镜反应的有_________种;
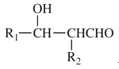
(5)![]() 是重要的工业加工助剂,写出以乙烯和乙醛为原料制备
是重要的工业加工助剂,写出以乙烯和乙醛为原料制备![]() 的合成路线。(其它无机试剂任选),(合成路线常用的表达方式为:A
的合成路线。(其它无机试剂任选),(合成路线常用的表达方式为:A B
B 目标产物)___________________
目标产物)___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活等密切相关,从化学视角回答下列问题:
(1)电闪雷鸣的雨天,空气中发生的化学反应会增加雨水的含氮量,有关反应的化学方程式是_____、_______、_________________。
(2)我国以煤炭为主的能源结构决定了我国的酸雨以硫酸型为主,为减少SO2的污染和酸雨的形成,目前常应用石灰法脱硫。过程如下:通过煅烧石灰石得到生石灰,以生石灰为脱硫剂,在吸收塔中与废气中的SO2反应而将硫固定,最终生成CaSO4,有关反应的化学方程式为_______、______、_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于密闭容器中的可逆反应:N2(g)+3H2(g)![]() 2NH3(g),400℃,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示.下列叙述正确的是
2NH3(g),400℃,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示.下列叙述正确的是
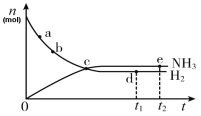
A. a点的正反应速率比b点的大B. c点处反应达到平衡
C. d点和e点处n(N2)不相等D. d点3v正(H2)= v逆(N2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答下列问题。该小组设计的简单实验装置如图所示:

该实验的主要操作步骤如下:
①配制100mL1.0molL﹣1的盐酸溶液;
②用_______(填仪器名称并注明规格)量取10.0mL1.0molL﹣1的盐酸溶液加入锥形瓶中;
③称取ag已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为______;
④往广口瓶中装入足量水,按如图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为VmL。
请将上述步骤补充完整并回答下列问题:
(1)用文字表述实验步骤④中检查装置气密性的方法:______。
(2)实验步骤⑤中应选用______(填序号)的量筒。
A.100mL B.200mL C.500mL
读数时除恢复到室温外,还要注意______。
(3)若忽略水蒸气的影响,在实验条件下测得气体摩尔体积的计算式为Vm=______,若未除去镁条表面的氧化膜,则测量结果______(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】误服铊盐会导致人体急性中毒,普鲁士蓝[KFe2(CN)6]可用作铊盐的解毒剂。
(1)Fe3+的价电子轨道表示式为___,与N同周期的主族元素中,第一电离能比N大的元素有___种。
(2)普鲁士蓝与硫酸作用可形成HCN,HCN的中心原子的杂化轨道类型为___,分子的立体构型是___,分子中σ键与π键数目之比为___。
(3)普鲁士蓝中的化学键不含有___(填字母)。
a.离子键
b.共价键
C.配位键
d.金属键
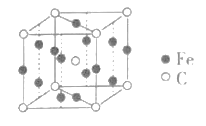
(4)已知FexCy的晶胞结构如图所示,则其化学式为___,铁原子的配位数是___。
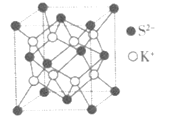
(5)如图为K2S的晶胞,该晶胞与CaF2晶胞结构相似,设晶体密度是ρg·cm-3,试计算K+与S2-的最短距离为___nm(阿伏加德罗常数用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC将合成化学元素第115号(Mc)提名为化学新元素,Mc的原子核最外层电子数是5,下列说法不正确的( )
A. Mc的原子核外有115个电子
B. Mc与N元素属于同一主族
C. Mc在同主族元素中金属性最强
D. 中子数为173的Mc核素符号是![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com