
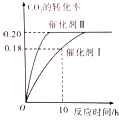
 已知CO2可生成绿色燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0 300℃时密闭容器中,当c(CO2)=1.00mol/L、c(H2)=1.60mol/L开始反应,结果如图所示,回答下列问题:
已知CO2可生成绿色燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0 300℃时密闭容器中,当c(CO2)=1.00mol/L、c(H2)=1.60mol/L开始反应,结果如图所示,回答下列问题:分析 (1)由图先计算二氧化碳的转化,根据v=$\frac{△c}{△t}$得用二氧化碳表示的反应速率,再根据速率之比=化学计量数之比,计算用氢气表示的反应速率;
(2)A、该反应两边都是气体,容器容积不变,所以密度始终不变;
B、充入稀有气体,不影响反应体系中各组分浓度,化学平衡不移动;
C、催化剂只影响反应速率,不影响化学平衡;
D、根据图示可知,在催化剂Ⅱ作用下的反应速率大于比催化剂Ⅰ作用下的反应速率;
(3)根据图中数据,利用“三段式”列式计算平衡时各组分的浓度,再根据k的概念列式带入计算;
(4)该反应为放热反应,温度升高,化学平衡向着逆向移动,化学平衡常数减小.
解答 解:(1)使用催化剂Ⅰ时,反应在10h内的二氧化碳的转化率为0.18,则二氧化碳转化了1.00mol/L×0.18=0.18mol/L,则v(H2)=3v(CO2)=3×$\frac{0.18mol/L}{10h}$=0.054 mol/(L•h),
故答案为:0.054 mol/(L•h);
(2)A、该反应前后气体的质量不变,容器的容积固定,所以混合气体的密度始终不变,故当容器内气体的密度不再改变时,反应不一定达到平衡状态,故A正确;
B、充入氩气增大压强,但是反应体系中各组分的浓度不变,化学平衡不发生移动,所以CO2的转化率不变,故B错误;
C、催化剂不影响化学平衡,所以CO2平衡转化率在上述反应条件下,催化剂Ⅱ与催化剂Ⅰ的转化率相等,故C错误;
D、在上述反应条件下,催化剂Ⅱ的反应速率大于催化剂Ⅰ的,说明催化剂Ⅱ比催化剂Ⅰ的催化效率高,故D正确;
故答案为:A、D;
(3)根据图中数据,平衡时二氧化碳的转化率为0.2,则二氧化碳转化了0.2mol/L,则
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始浓度:1 1.6 0 0
转化浓度:0.2 0.6 0.2 0.2
平衡浓度:0.8 1 0.2 0.2
化学平衡常数k=$\frac{0.2×0.2}{0.8×1^3}$=0.05 (mol/L)-2,
故答案为:0.05 (mol/L)-2;
(4)由于该反应为放热反应,温度增大,化学平衡向着逆向移动,反应物浓度减小,生成物浓度增大,化学平衡常数增大,故平衡常数K(400℃)<K(300℃).
故答案为:<.
点评 本题考查了化学反应速率、化学平衡常数的计算、影响化学反应速率因素等知识,题目难度中等,注意掌握化学反应速率、化学平衡常数的表达式及三段式的计算.


科目:高中化学 来源: 题型:选择题
| A. | 14462Sm与15062Sm 是同一种核素 | |
| B. | 14462Sm与15062Sm 互为同位素 | |
| C. | 14462Sm与15062Sm 的质量数相同 | |
| D. | 14462Sm与15062Sm 的核外电子数和中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
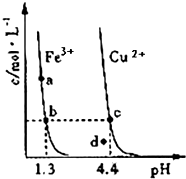 某温度下,将Fe(OH)3(s)、Cu(OH)2(s)分别置于蒸馏水中达到沉淀溶解平衡后,金属阳离子浓度随溶液pH的变化如图所示.下列判断正确的是( )
某温度下,将Fe(OH)3(s)、Cu(OH)2(s)分别置于蒸馏水中达到沉淀溶解平衡后,金属阳离子浓度随溶液pH的变化如图所示.下列判断正确的是( )| A. | 该温度下,Ksp[Fe(OH)3]>Ksp[Cu(OH)2] | |
| B. | c、d 两点代表的溶液中c(H+) 与c(OH-) 乘积不相等 | |
| C. | Cu(OH)2在c点比在d点代表的溶液中溶解程度小 | |
| D. | 加适量浓NH3•H2O可使溶液由a点变到b点 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 名称 | 相对分子质量 | 性状 | 熔点 | 沸点 | 密度 | 溶解度 | ||
| 水 | 乙醇 | 乙醚 | ||||||
| 甲苯 | 92 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 易溶 | 易溶 |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 | 易溶 |
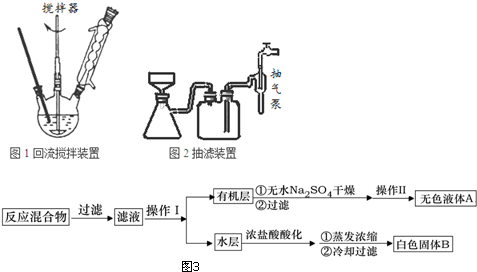
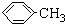 ;操作Ⅱ为蒸馏.
;操作Ⅱ为蒸馏.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
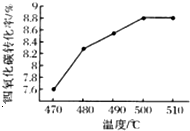 SiCl4在室温下为无色液体,易挥发,有强烈的刺激性.把SiCl4先转化为SiHCl3,再经氢气还原生成高纯硅.
SiCl4在室温下为无色液体,易挥发,有强烈的刺激性.把SiCl4先转化为SiHCl3,再经氢气还原生成高纯硅.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
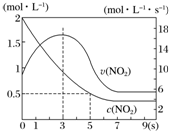 某绝热恒容容器中充入2mol•L-1 NO2,发生反应2NO2(g)═N2O4(g)△H=-56.9kJ•mol-1.下列分析不正确的是( )
某绝热恒容容器中充入2mol•L-1 NO2,发生反应2NO2(g)═N2O4(g)△H=-56.9kJ•mol-1.下列分析不正确的是( )| A. | 5s时NO2的转化率为75% | |
| B. | 0~3 s时v(NO2)增大是由于体系温度升高 | |
| C. | 3s时化学反应处于平衡状态 | |
| D. | 9s时再充入N2O4,平衡后K较第一次平衡时大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
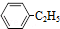 (g)?
(g)? (g)+H2(g)△H=akJ•mol-1,经一段时间后达到平衡,反应过程中测定的部分数据见表:
(g)+H2(g)△H=akJ•mol-1,经一段时间后达到平衡,反应过程中测定的部分数据见表:| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(乙苯)/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
| n(苯乙烯)/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
| A. | 反应在前20min的平均速率为v(H2)=0.008mol•L-1•min-1 | |
| B. | 保持其他条件不变,升高温度,平衡时,c(乙苯)=0.08 mol•L-1,则a<0 | |
| C. | 保持其他条件不变,平衡后向容器中再充入0.40mol乙苯,再次达到平衡时乙苯的转化率小于50.0% | |
| D. | 相同温度下,起始时向容器中充入0.10 mol乙苯、0.10 mol苯乙烯和0.30 molH2,达到平衡前v(正)>v(逆) |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com