
| A. | 溶液中Pb2+和I-浓度都增大 | B. | 溶度积常数Ksp增大 | ||
| C. | 沉淀溶解平衡向逆向移动 | D. | PbI2的溶解度不变 |
分析 含有大量PbI2的饱和溶液中存在着平衡PbI2(s)?Pb2+(aq)+2I-(aq),加入KI溶液,c(I-)增大,沉淀溶解平衡逆移,c(Pb2+)减小,溶度积常数Ksp只与温度有关.
解答 解:A、含有大量PbI2的饱和溶液中存在着平衡PbI2(s)?Pb2+(aq)+2I-(aq),加入KI溶液,c(I-)增大,沉淀溶解平衡逆移,c(Pb2+)减小,故A错误;
B、溶度积常数Ksp只与温度有关,改变c(I-)Ksp不变,故B错误;
C、含有大量PbI2的饱和溶液中存在着平衡PbI2(s)?Pb2+(aq)+2I-(aq),加入KI溶液,c(I-)增大,沉淀溶解平衡左移,故C正确;
D、加入KI溶液,c(I-)增大,沉淀溶解平衡逆移,c(Pb2+)减小,PbI2的溶解度减小,故D错误;
故选C.
点评 本题考查了沉淀溶解平衡的移动、影响Ksp的因素,注意Ksp是温度的函数不随浓度的变化而变化,题目难度不大.


科目:高中化学 来源: 题型:填空题
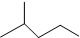 表示的分子式C6H14;名称2-甲基戊烷.
表示的分子式C6H14;名称2-甲基戊烷.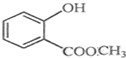 中含有的官能团的名称为酚羟基、酯基.
中含有的官能团的名称为酚羟基、酯基. .3-甲基-2-乙基-1-戊烯结构简式为CH3CH(CH3)CH2C(CH2CH3)=CH2.
.3-甲基-2-乙基-1-戊烯结构简式为CH3CH(CH3)CH2C(CH2CH3)=CH2.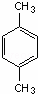 名称为对二甲苯.
名称为对二甲苯.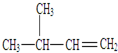 名称为3-甲基-1-丁烯.
名称为3-甲基-1-丁烯.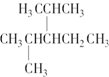 名称为2,4-二甲基-3--乙基戊烷.
名称为2,4-二甲基-3--乙基戊烷.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
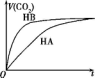 等体积、浓度均为0.2mol•L-1的三种溶液:①HA溶液、②HB溶液、③NaHCO3溶液,已知将①②分别与③混合,实验测得所产生的CO2气体体积(V)随时间(t)变化如图所示.下列说法不正确的是( )
等体积、浓度均为0.2mol•L-1的三种溶液:①HA溶液、②HB溶液、③NaHCO3溶液,已知将①②分别与③混合,实验测得所产生的CO2气体体积(V)随时间(t)变化如图所示.下列说法不正确的是( )| A. | 酸性:HB>HA>H2CO3 | |
| B. | 反应结束后所得两溶液中:c(A-)>c(B-) | |
| C. | 上述三种溶液中由水电离的c(OH-)相对大小:NaHCO3>HA>HB | |
| D. | HA溶液和NaHCO3溶液反应所得的溶液中:c(A-)+c(HA)=0.1 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
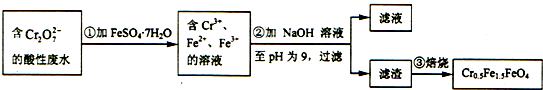
| A. | 根据第①步反应可知还原性:Cr3+大于Fe2+ | |
| B. | 第②步过滤得到的滤渣中主要成分为Cr(OH)3、Fe(OH)2,不含Fe(OH)3 | |
| C. | 欲使1L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4,理论上需要加入27.8g FeSO4•7H2O | |
| D. | 第③步高温焙烧过程用到的主要实验仪器中属于硅酸盐质的有:酒精灯、蒸发皿、泥三角 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
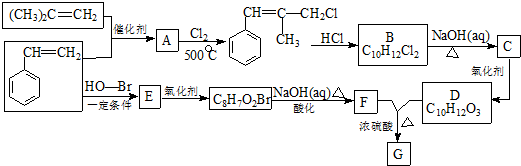
 .
.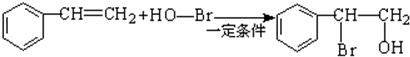 .
.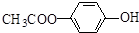 和
和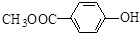 .
.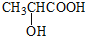 ) 的合成路线:
) 的合成路线: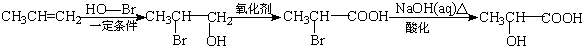 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只含一种分子的物质是纯净物,只含一种元素的物质也是纯净物 | |
| B. | 医疗上的血液透析利用了胶体的性质 | |
| C. | NH3溶于水后所得的溶液可以导电,所以NH3为电解质 | |
| D. | 从海水中可以得到NaCl,电解NaCl溶液可制备Na |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制一定物质的量浓度的溶液时,容量瓶必须洁净、干燥,不漏水 | |
| B. | 实验室里需要480 mL 2.0 mol/L的氢氧化钠溶液,配制该溶液时先称量氢氧化钠固体38.4 g,然后再按照溶解、冷却、移液、定容、摇匀的步骤进行操作 | |
| C. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液的浓度偏大 | |
| D. | 实验室配制500 mL 0.2 mol/L的硫酸亚铁溶液,其操作是用天平称量27.8 g绿矾,将其放入500 mL容量瓶,加水溶解、稀释、定容、摇匀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com