
 ��
��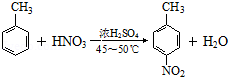 ����Ӧ�ܵĻ�ѧ����ʽΪ
����Ӧ�ܵĻ�ѧ����ʽΪ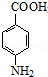 +CH3CH2OH
+CH3CH2OH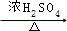
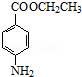 +H2O��
+H2O��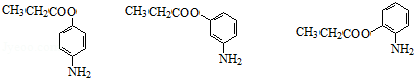 ������дһ�֣�
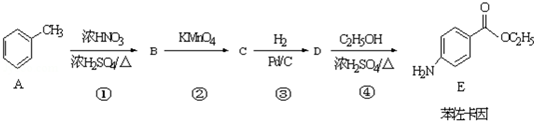
������дһ�֣� ���� �������и���ת����ϵ�����E�Ľṹ��֪���ױ�����������Ӧ����BΪ ��B����������Ӧ����CΪ
��B����������Ӧ����CΪ
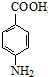 ��D����������Ӧ����E���Դ˽����⣮
��D����������Ӧ����E���Դ˽����⣮
��� �⣺��1����������ķ�����֪��BΪ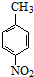 ��
��
�ʴ�Ϊ�� ��
��
��2����Ӧ�ڵķ�Ӧ����Ϊ������Ӧ����Ӧ�ܵķ�Ӧ����Ϊ������Ӧ��
�ʴ�Ϊ��������Ӧ��������Ӧ��
��3����Ӧ�ٵĻ�ѧ����ʽΪ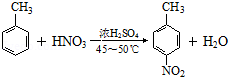 ����Ӧ�ܵĻ�ѧ����ʽΪ
����Ӧ�ܵĻ�ѧ����ʽΪ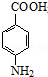 +CH3CH2OH
+CH3CH2OH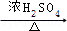
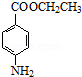 +H2O��
+H2O��
�ʴ�Ϊ�� ��
�� +CH3CH2OH
+CH3CH2OH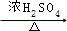
 +H2O��
+H2O��
��4�����ݱ�������Ľṹ��ʽ��֪����˴Ź�����������5���壬
�ʴ�Ϊ��5��
��5�����������ٺ������Ұ���ֱ���뱽���������ڱ�����������ȡ�������ۺ����������������ı��������ͬ���칹��Ϊ��������-NH2��-C3H5O2���ţ�-C3H5O2�������������Ľṹ��-OOCCH2CH3��-CH2OOCCH3��-CH2CH2OOCH��-CH��CH3��OOCH��-COOCH2CH3��-CH2COOCH3�������백�����л�Ϊ�ڡ��䡢������λ��λ�ù�ϵ�����Թ���18�ֽṹ�����˱��������⣬��17�֣���������NaOH��Һ��Ӧ����2�����ε�ͬ���칹��Ľṹ��ʽΪ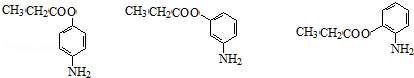 ��
��
�ʴ�Ϊ��17�� ������һ�֣���
������һ�֣���
���� ������Ҫ�������л����ƶ���ϳɣ�Ϊ��Ƶ����ͳ������ͣ��е��Ѷȣ����� ʱע���л�������֮����ת������Ӧ��������������û���֪ʶ���������������Ϣ�ǽ���Ĺؼ�����5��Ϊ�״��㣮


 �������Ͽ��㱾ϵ�д�
�������Ͽ��㱾ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �϶���Al3+��Mg2+��Cl- | B�� | �϶���Al3+��Mg2+��NH4+��Cl- | ||
| C�� | �϶���HCO3-��K+��MnO4- | D�� | �϶���Al3+��Mg2+��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫʳƷ�Dz����κλ�ѧ���ʵ�ʳƷ | |
| B�� | ����ij����ʱ��������ֱ�ӹ۲쵽����ʻ�ɫ������жϸ�����һ������Ԫ�� | |
| C�� | ��þ�����ڿ����г��ȼ�գ����Եõ����ֹ��� | |
| D�� | ��ȡ���������������ۣ��ֱ���������ϡHCl������NaOH��Һ����ų������������ȣ�ͬ��ͬѹ�£� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
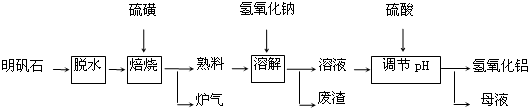
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
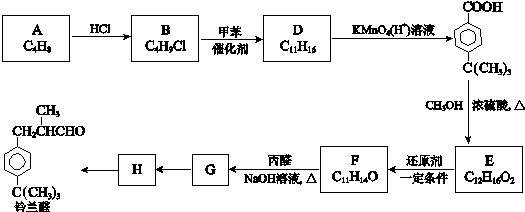
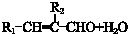
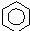 $\stackrel{����}{��}$
$\stackrel{����}{��}$ 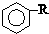 +HCl
+HCl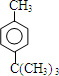 ��
�� ��
��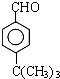 ��
��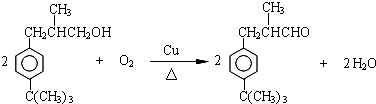 ��
��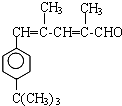 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.6 | B�� | 0.333 | C�� | 0.4 | D�� | 0.36 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���߾��ж����ЧӦ | B�� | ���߾�������Ĥ | ||
| C�� | ��ɢ�����ӿ�ͨ����ֽ | D�� | ���������ȳ���������ܽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.4mol | B�� | ��0.2mol | ||
| C�� | ����0.2mol | D�� | ����0.2mol����0.4mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1mol��ϩ���к���˫������ĿΪ0.1NA | |
| B�� | 1mol/L FeCl3��Һ�У�������������������0.4NA | |
| C�� | 12g���ʯ��������C-C����Ϊ2NA | |
| D�� | 18g��D2O��NA��CH3-������ͬ�ĵ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com