

���� ��1���Ȼ���ˮ������ԭ������Ȼ��⣬�¶�Խ�ߣ��Ȼ����ˮ������Խ���Ȼ���Ļӷ�Խǿ������������ʽ��Ӽ�������SiCl4�Ʊ�����Ȼ�ѧ����ʽ��ע���ʱ������Ӧ�ĸı䣻
��2�������ʱ���ɵ�BaCl2��̼�ᱵ�ܽ����������ᷴӦ���ɵģ�
��3����������������������þ��ȫ����������Һ��PHֵ�����������ܽ�����¶�����Сȷ������A�ijɷ֣������¶���Ϊ�˳�ȥ�����ӣ�
��4�����ݴ���Һ����������ķ����Լ��������ε�����Ϊ�����������������
��� �⣺��1���Ȼ���ˮ������ԭ������Ȼ��⣬ˮ�ⷽ��ʽΪ��SiCl4+4H2O=H4SiO4��+4HCl���¶ȸ�ʱ���Ȼ����ˮ�����������Ȼ���Ļӷ���ǿ�����Ȼ�������Ⱦ�������¶Ƚϵ�ʱ���ܷ�ֹHCl�ӷ���Ⱦ���������SiCl4��ˮ�����ʣ���ֹ��Ӧ���ھ��ң�
��SiCl4��s��+H2��g���TSiHCl3��s��+HCl��g����H1=47kJ•mol-1
��SiHCl3��s��+H2��g���TSi��s��+3HCl��g����H2=189kJ•mol-1
���ݸ�˹���ɣ��ɢ�+�ڿɵã�SiCl4��s��+2H2��g��=Si��s��+4HCl��g����H=+236 kJ•mol-1
�ʴ�Ϊ���ܷ�ֹHCl�ӷ���Ⱦ���������SiCl4��ˮ�����ʣ�SiCl4��s��+2H2��g��=Si��s��+4HCl��g����H=+236 kJ•mol-1��
��2��̼�ᱵ�����ᷴӦ�����Ȼ�������Ӧ�����ӷ���ʽΪ��BaCO3+2H+=Ba2++CO2+H2O����
�ʴ�Ϊ��BaCO3+2H+=Ba2++CO2��+H2O��
��3����pH=3.4ʱ����������ȫ���ɳ�������pH=12.4ʱ��þ������ȫ��������������þ��Mg��OH��2�����Ե�pH=12.5ʱ������A�ijɷ���������þ���������ƣ������¶�70���Ŀ����ȷ����������ȫ��ȥ��
�ʴ�Ϊ��Mg��OH��2��Ca��OH��2��ȷ����������ȫ��ȥ�����¶�Խ�ߣ�Ca��OH��2�ܽ��ԽС����
��4������Һ����ȡ����ķ����ǣ�����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ�ʵ����������Ũ���õ��ĺ������ε�������Ϊ�������������������������ƾ��ƣ�
�ʴ�Ϊ��3��
���� ���⿼���Ʊ�ʵ�鷽�������ʷ�����ᴿ�����������Ʒ��������ۡ���ѧ����ȣ���ֿ�����ѧ���ķ���������������֪ʶǨ�����õ��������Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
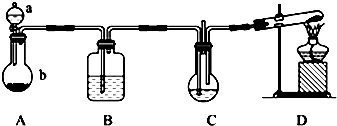
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
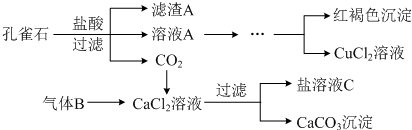
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ķ���ʽ��P | B�� | ������Ľṹʽ��H-Cl-O | ||
| C�� | �����ӵĽṹʾ��ͼ�� | D�� | ��������ĵ���ʽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ͨ��ˮ�У�Cl2+H2O?2H++Cl-+ClO- | |
| B�� | KI��Һ��H2SO4�ữ��H2O2��Һ��ϣ�2 I-+H2O2+2 H+=2 H2O+I2 | |
| C�� | ��NH4HCO3��Һ�еμӹ���Ba��OH��2��Һ��HCO3-+OH-+Ba2+=H2O+BaCO3�� | |
| D�� | �������������Һ���ն�������SO2+MnO4-+4H+=SO42-+Mn2++2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3��2��2 | B�� | 1��2��3 | C�� | 1��3��3 | D�� | 3��1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2���ӱ���ģ�ͣ�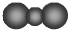 | |
| B�� | ����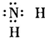 | |
| C�� | ԭ�ӽṹʾ��ͼ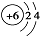 ��ʾ12C��Ҳ���Ա�ʾ14C ��ʾ12C��Ҳ���Ա�ʾ14C | |
| D�� | ��Ȳ�����ʽ CH��CH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
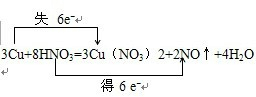 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCl | B�� | Na2SO4 | C�� | NaCl | D�� | CuSO4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com