
�����й�ʵ��������У���ȷ����
����ʪ���pH��ֽ�ⶨ��Һ��pH
�ڲ����ô����������������ƹ����̼���ƹ���
�ۿ��ü��ȷ�����I2��NH4Cl�Ļ����
�ܿ���ϡ����ϴ�ӡ�������Ӧ��ʵ��������Թܱ��ϵ���
���������ˮ�ɳ�ȥ���е�Ca(HCO3)2
��ʵ���������Ȼ�������Һʱ�����Ƚ��Ȼ������ܽ��������У��ټ�������ˮϡ�ͣ���������������
A���ڢܢ� B���ڢۢ� C���ڢܢݢ� D���ڢۢܢݢ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶������У��ģ���ѧ�Ծ��������棩 ���ͣ��ƶ���
��ͼA��H��Ϊ��ѧ��ѧ����������ʣ�����֮��������ת����ϵ������A��C��Ϊ�������ʣ�C��ˮ��Ӧ����D����������壬D��H����ɫ��Ӧ���ʻ�ɫ����ͨ��״����E�����������NaOH��������ɷ������ֽⷴӦ������Ӧ���������ɵ�ˮ��������������ȥ��
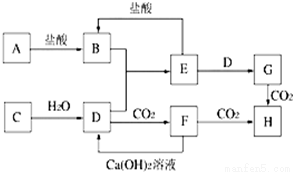
��ش��������⣺
��1��B��_______��H��________�����ѧʽ��
��2��д��Eת��ΪG�����ӷ���ʽ________��
��3��H�ڼ����·�Ӧ����F��д���˷�Ӧ�Ļ�ѧ����ʽ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������и�һ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������ָ����Һ�У�����һ���ܴ���������ǣ� ��
A������H+�������������Һ�У�SO32-��Ba2+��K+��NO3-
B��ʹ��̪�Ժ�ɫ����Һ�У�NO3-��Cl-��K+��Ba2+
C�������۷ų���������Һ�У�Na+��H+��CH3COO-��Cl-
D�������Ե���ɫ��Һ�У�K+��Fe2+��NO3-��SO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʦ���У��Ž�һ�и��������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�ʵ������������ͺͽ��۶���ȷ���ǣ� ��
| �� �� | �� �� | ���͡����� |
A | ������Fe���м��������ַ�Ӧ������KSCN��Һ | ��Һ�ʺ�ɫ | ϡ���ὫFe����ΪFe3+ |
B | ��Na2CO3��Һ��ͨ������CO2 | ��Һ����� | ������Na2CO3���� |
C | Al������ϡ������ | ������ | Al�������жۻ����γ����ܵ�����Ĥ |
D | �ò�����պȡŨ��ˮ�㵽��ɫʯ����ֽ�� | ��ֽ����ɫ | Ũ��ˮ�ʼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016����������һ��ѧ�����ϵ������¿�����ѧ�Ծ��������棩 ���ͣ������
��ˮ���̲��ŷḻ����Դ����ˮ�ۺ����õ�����ͼ���¡�

��1����NaCl��ԭ�Ͽ��Եõ����ֲ�Ʒ��
�ٹ�ҵ����NaCl�Ʊ������ƵĻ�ѧ����ʽ��
��ʵ�����ö��Ե缫���100 mL0.1 mol/LNaCl��Һ���������������õ�112 mL���壨��״��������������Һ��pHΪ__________�����Է�Ӧǰ����Һ������仯����
�۵���Ȼ���ϡ��Һ���Ʊ���84����Һ����ͨ��ʱ��������Һ��ȫ���գ�����������Һ����һ�����ʣ�д����Ӧ�Ļ�ѧ����ʽ�� ��
��2����������κ��±ˮ���̺��ŷḻ��þ��Դ����������;���ɻ�ý���þ��
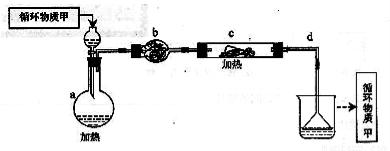
±ˮ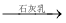 Mg��OH��2
Mg��OH��2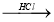 MgCl2��Һ��MgCl2��6H2O��MgCl2
MgCl2��Һ��MgCl2��6H2O��MgCl2 Mg
Mg
���У���MgCl2��6H2O��ȡ��ˮMgCl2�IJ���װ�ã�����̨���ƾ������ԣ����£�
����ͼ�У�װ��a�� �� ��˫�����͵������
��ѭ�����ʼ�������
����ȡ��ˮ�Ȼ�þ�������Ȼ�����ڵ������½��У�ԭ����
��װ��b���������ʿ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲������ɽ��������ͭ����У�����ϵ�����������ѧ�Ծ��������棩 ���ͣ������
����β����Ϊ������Ⱦ����Ҫ��Դ֮һ�����к��д������к����ʣ�����CO��NOx��̼�⻯����������������ȡ�������β��������ʹ���������������˾����ս���Իش��������⣺
��1����CH4����ԭNOx�������������������Ⱦ����֪��
��CH4��g��+4NO��g���T2N2��g��+CO2��g��+2H2O��g����H=-1160kJ•mol-1
��CH4��g��+4NO2��g���T4NO��g��+CO2��g��+2H2O��g����H=-574kJ•mol-1
����CH4��NO2��ɻ�ԭ��N2������CO2��ˮ�������Ȼ�ѧ����ʽ��____________________��
��2��NOxҲ�ɱ�NaOH��Һ���ն�����NaNO3��NaNO2����֪ij�¶��£�HNO2�ĵ��볣��Ka=9.7��10-4mol•L-1��NO2-��ˮ�ⳣ��ΪKh=8.0��10-10mol•L-1������¶���ˮ�����ӻ�����=______���ú�Ka��Kh�Ĵ���ʽ��ʾ������ʱ��Һ���¶�______25�棨������������������=������
��3������������CO�ϳɼ״�����Ӧ���Ȼ�ѧ����ʽΪ��CO��g��+2H2��g�� CH3OH��g����H=-90.8KJ•mol-1����ͬ�¶��£�CO��ƽ��ת��������ͼ��ʾ��ͼ��T1��T2��T3�ĸߵ�˳����________��������______��
CH3OH��g����H=-90.8KJ•mol-1����ͬ�¶��£�CO��ƽ��ת��������ͼ��ʾ��ͼ��T1��T2��T3�ĸߵ�˳����________��������______��

��4�������ϻ���������CH3OH����CH3OCH3���������Ϊ1.0L�ĺ����ܱ������з�����Ӧ��2CH3OH(g) CH3OCH3(g)+H2O(g)��
CH3OCH3(g)+H2O(g)��
������� | �¶ȣ��棩 | ��ʼ���ʵ�����mol�� | ƽ�����ʵ�����mol�� | |
CH3OH | CH3OCH3 | H2O | ||
�� | 387 | 0.20 | 0.080 | 0��080 |
�� | 207 | 0.20 | 0.090 | 0.090 |
�÷�Ӧ������ӦΪ________��Ӧ������ȡ��������ȡ���������ʼ�����������г���CH3OH0.15mol��CH3OCH30.15mol��H2O0.10mol����Ӧ����_____������У�����������桱����
��5��CH3OHȼ�ϵ���ڱ�ЯʽͨѶ�豸���������������Ź㷺��Ӧ�á���֪��ع���ʱ���ܷ�Ӧ����ʽΪ��2CH3OH+3O2=2CO2+4H2O����ع���ʱ��ʾ��ͼ����ͼ��ʾ��
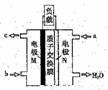
���Ӵ�������Ĥ����_____�缫�����M������N�����������ĵ缫��ӦʽΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������������������ѧ��һ��10�»�ѧ���������棩 ���ͣ�ѡ����
ͬ��ͬѹ��,1���X2������3���Y2���廯������2������廯����Z,����Z�Ļ�ѧʽ�ɱ�ʾΪ
A��XY3 B��XY C��X3Y D��X2Y3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ��ƶ���
����ԭ���������������W��T��X��Y��Z��R����ǰ������Ԫ�أ�TW3��ʹʪ��ĺ�ɫʯ����ֽ����ɫ��X��Yλ��ͬһ������Y��ԭ��������X��2����Z��R�������г���������Z��R�������ڳ�ʪ�����зֱ����ɺ��ɫ�����ɫ�⣮
��ش��������⣺
��1��TW3�ĵ���ʽΪ ��
��2����W��T��X��Y�е�Ԫ�����һ�����ӻ�����M���ܷ�����ͼת����ϵ��
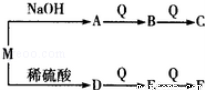
F��E����Է�������֮��Ϊ16����M�Ļ�ѧʽ����Ϊ ��
C��ˮ��Ӧ�Ļ�ѧ����ʽΪ ��
��3����TW4��2Y2X8�ܺ�ZYX4��ˮ��Һ�з�Ӧ����Z2+��YX42����д�����ӷ���ʽ ��
��4�������£���WTX3Ũ��Һ����Z��RΪ��幹��ԭ��أ����������� ��
������ӦʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ����ϳ���ʯ�ŵ�һ��ѧ�߶��������Ļ�ѧ���������棩 ���ͣ�ѡ����
�±�Ϊij�����ڲ�ͬ����ʱ�������Ŀ�����Ⱦ��������������ƽ����ʻ1������㣩��
��Ⱦ��/g•km��1 | ����/ km•h��1 | ||
50 | 80 | 120 | |
һ����̼ ���������� ̼�⻯���� | 8.7 0.6 0.7 | 5.4 1.5 0.6 | 9.6 3.8 0.8 |
�����ϱ�������˵������ȷ����
A��������ʻʱ����Ⱦ����CO�������
B����������Ϊ120km•h��1ʱ����Ⱦ������
C���ӻ����Ƕȿ��ǣ�����ʵ������� ��Ϊ50 km•h��1
��Ϊ50 km•h��1
D��������������ʱ�������ĵ������� ��Ҳ��֮����
��Ҳ��֮����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com