
| A. | HF | B. | Na2O2 | C. | CaCl2 | D. | H2SO4 |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,碱金属族、碱土金属族元素和氧族、卤族元素之间易形成离子键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,据此分析解答.
解答 解:A.HF中H-F原子之间只存在共价键,为共价化合物,故A错误;
B.过氧化钠中钠离子和过氧根离子之间存在离子键、过氧根离子之间O-O原子之间存在共价键,为离子化合物,故B正确;
C.氯化钙中钙离子和氯离子之间只存在离子键,不含共价键,故C错误;
D.硫酸分子中S-O、O-H原子之间只存在共价键,为共价化合物,故D错误;
故选B.
点评 本题考查离子键和共价键判断,侧重考查基本概念,明确物质构成微粒及微粒之间作用力即可解答,注意不能根据是否含有金属元素判断离子键,易错选项是C.


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:选择题

| A. | 溶液甲中一定含有K2SiO3、NaNO2,可能含有KAlO2、K2CO3 | |
| B. | 由于在溶液甲中加入足量稀盐酸后再加入BaCl2溶液,因此无法判断溶液中是否有K2SO3 | |
| C. | 气体A和气体D一定均为纯净物 | |
| D. | 原混合物中一定含有MnO2、Fe2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ①③ | C. | ③④ | D. | ②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数X>Y | B. | 原子半径X<Y | ||
| C. | X和Y一定同周期 | D. | X是第ⅡA族元素,Y是第VⅡA族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
;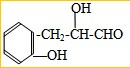 或
或 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | 实验目的 | T/℃ | NO初始浓度mol/L | CO初始浓度mol/L | 同种催化剂的比表面积m2/g |
| Ⅰ | 为以下实验作参照 | 280 | 6.50×10-3 | 4.00×10-3 | 80 |
| Ⅱ | 6.50×10-3 | 4.00×10-3 | 120 | ||
| Ⅲ | 探究温度对反应速率的影响 | 360 | 80 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
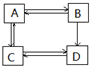
| A. | A的相对分子质量小于C、D的相对分子质量而大于B的相对分子质量 | |
| B. | 若A为2-丙醇,则其可实现如右图的所有转化 | |
| C. | 若A、B、D、为链状化合物,则C也一定为链状化合物 | |
| D. | C→A的反应类型为加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
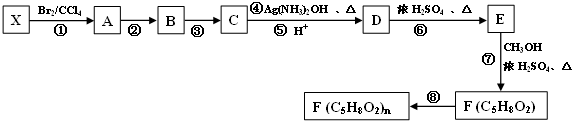
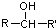 $\stackrel{[O]}{→}$
$\stackrel{[O]}{→}$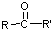 ,
,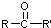 不易被氧化成羧酸
不易被氧化成羧酸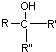 不易被氧化成醛或酮
不易被氧化成醛或酮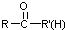 $\stackrel{HCN}{→}$
$\stackrel{HCN}{→}$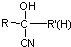 $\stackrel{H^{+}/H_{2}O}{→}$
$\stackrel{H^{+}/H_{2}O}{→}$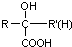 (R、R′、R″均代表烃基 )
(R、R′、R″均代表烃基 )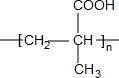 ;
; ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com