
【题目】除去FeCl2溶液中的FeCl3所需试剂是( )
A.Cl2B.CuC.FeD.NaOH
科目:高中化学 来源: 题型:
【题目】反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,试回答:
(1)增加Fe的量,其反应速率________(填“增大”、“不变”或“减小”,下同)。
(2)将容器的体积缩小一半,其反应速率____________。
(3)保持体积不变,充入N2使体系压强增大,其反应速率____________。
(4)保持压强不变,充入N2使容器的体积增大,其反应速率____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“嫦娥一号”探月成功,实现了中国人“奔月”的梦想。
(1)“嫦娥一号”使用的推进剂是液氢和液氧,这种推进剂的优点是____________________________;_______________________________。(请写两条)
(2)已知:①H2(g)+1/2O2(g)===H2O(l)
ΔH1=-285.8 kJmol-1
②H2(g)===H2(l) ΔH2=-0.92 kJmol-1
③O2(g)===O2(l) ΔH3=-6.84 kJmol-1
④H2O(l)===H2O(g) ΔH4=44.0 kJmol-1
请写出液氢和液氧生成气态水的热化学方程式:__________________________。
如果此次“嫦娥一号”所携带的燃料为45 t,液氢、液氧恰好完全反应生成气态水,总共释放的热量为________kJ(保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸厂拟用烟气处理含Cr2O72﹣的酸性废水,在脱硫的同时制备Cr2O3产品.具体流程如下: 
已知吸收塔中反应后的铬元素以Cr3+形式存在,下列说法中正确的是( )
A.吸收塔中的硫元素可能以单质形式存在
B.中和池中只发生生成沉淀的复分解反应
C.在中和池中加入盐酸酸化的BaCl2溶液,可能产生白色沉淀
D.由题意分析得到,沉淀可能是Cr(OH)6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
[实验一 焦亚硫酸钠的制取]
采用下图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2=Na2S2O5。
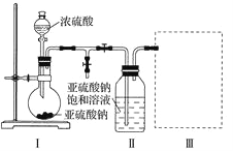
(1)装置Ⅰ中产生气体的化学方程式为____________________________________。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是____________________。
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________(填字母)。
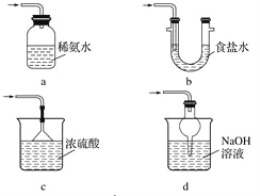
实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是________(填序号)。
a.测定溶液的pH
b.加入Ba(OH)2溶液
c.加入盐酸
d.加入品红溶液
e.用蓝色石蕊试纸检测
(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】广东正在建设海洋强省。下列说法不正确的是( )
A.从海带中提取碘单质的过程涉及氧化还原反应
B.往淡水中加入NaCl等配成的人造海水,可用于海产品的长途运输
C.赤潮主要是由工农业生产和生活废水引起沿海水域的富营养化而造成的
D.海洋经济专属区的资源开发可获得Fe、Co、K、Au、Mg、B等金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾广泛用作氧化剂。现有一个氧化还原反应的体系中共有KMnO4、MnSO4、H2O、Fe2(SO4)3、
FeSO4、H2SO4、K2SO4七种物质。
Ⅰ.写出一个包含上述七种物质的氧化还原反应方程式(需要配平):____________。
Ⅱ.某研究性学习小组根据上述反应设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1mol/L,溶液的体积均为200mL,盐桥中装有饱和K2SO4溶液。

回答下列问题:
(1)此原电池的正极是石墨__________(填“a”或“b”),发生________反应。
(2)电池工作时,盐桥中的SO42-移向________(填“甲”或“乙”)烧杯。
(3)乙烧杯中的电极反应式分别为__________________。
(4)若不考虑溶液的体积变化,MnSO4浓度变为1.5 mol·L-1,则反应中转移的电子为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向2L密闭容器中加入2molN2和10molH2,发生反应N2(g)+3H2(g)![]() 2NH3(g),2min时测得剩余N2为1mol,下列化学反应速率表示不正确的是( )
2NH3(g),2min时测得剩余N2为1mol,下列化学反应速率表示不正确的是( )
A. v(N2)=0.25 mol·L-1·min-1
B. v(H2)=0.75 mol·L-1·min-1
C. v(NH3)=1 mol·L-1·min-1
D. v(NH3)=0.5 mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com