
X、Y、Z是中学化学中常见的单质或化合物,且X、Y、Z均含有同一种元素,它们能实现如图所示的转化关系(其他物质省略):
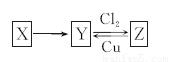
(1)若X是一种生活中使用量最大的金属单质,写出Z与Cu反应的离子方程式__________________。
(2)若X是一种非金属单质,常温下为固体;Y是一种能使品红溶液褪色且加热后又能恢复原来颜色的化合物。写出Z和Cu反应的化学方程式_________________________________。
科目:高中化学 来源:2015-2016学年江苏省高一创新班下期末化学试卷(解析版) 题型:实验题
I.为了探究外界条件对H2O2分解速率的影响,有同学利用实验室提供的仪器和试剂进行了如下实验,请填写下列空白:
试剂:5%H2O2溶液,10%H2O2溶液,1mol/LFeCl3溶液,MnO2粉末
仪器:试管、胶头滴管、酒精灯
(1)实验目的:探究温度对化学反应速率的影响
实验步骤:分别对A、B两支试管中加入5mL 5%H2O2溶液,将试管A放入5℃水浴中,将试管B放入40℃水浴中,同时分别向两试管中加入2~3滴1mol/LFeCl3溶液。观察实验现象。
实验现象:试管________(填“A”或“B”)中产生气泡的速率快,说明___________。
(2)实验目的:探究浓度对化学反应速率的影响
实验步骤:向试管A中加入5mL 5%H2O2溶液,向试管B中加入5mL 10%H2O2溶液,观察实验现象。
实验现象:试管A、B中均有少量气体缓慢产生。
请你改进实验方案,使该实验的实验现象更为明显,以支撑“浓度改变会影响化学反应速率”这一理论预测,___________________________。
(3)实验目的:________________________。
实验步骤:分别向试管A和B中加入5mL 5%H2O2溶液后,再向试管B中加入1mL 1mol/L的FeCl3溶液,观察实验现象。
你认为方案(3)的设计是否严谨?_________(填是或否),说明理由_________________。
II.请设计“以镁与不同浓度稀硫酸反应探究浓度对化学反应速率影响”的实验方案。
实验中可供选择的试剂与用品:镁带(密度1.74g/cm、宽度0.5cm、厚度0.05cm)、砂纸、剪刀、1.0mol/L的硫酸、蒸馏水、恒温水浴箱、试管、量筒、秒表。实验方案:_____________________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都外国语学校高一下期末理科化学卷(解析版) 题型:选择题
下列有关叙述正确的是
A. 元素性质呈周期性变化的根本原因是元素化合价呈周期性变化
B. BF3和CO2分子中所有原子均满足最外层为8电子结构
C. 已知114号元素的一种核素的质量数为298,则该元素的相对原子质量为298
D. [14NH3T]+中,电子数、质子数、中子数之比为10:11:9
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:选择题
甲~辛等元素在周期表中的相对位置如下表,甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素。下列判断正确的是
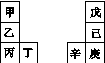
A. 金属性:甲>乙>丁
B. 原子半径:辛>戊>己
C. 丙与庚的原子核外电子数相差13
D. 乙的单质在空气中燃烧生成只含离子键的化合物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期末化学试卷(解析版) 题型:推断题
【加试题】某研究小组以烃A为主要原料,采用以下路线合成药物X和高聚物Y:
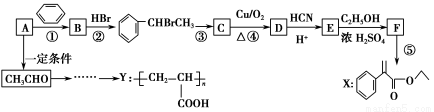
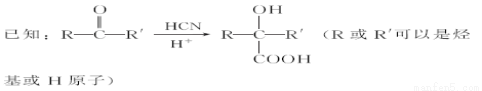
请回答下列问题:
(1)若反应①、②的原子利用率均为100%,则A的名称为________。
(2)反应③的条件是________________,反应⑤的反应类型是________________。
(3)写出反应④的化学方程式________________________________________。
(4)写出同时符合下列条件的E的所有同分异构体的结构简式:___________________。
ⅰ.属酚类化合物,且是苯的对位二取代物;ⅱ.能发生银镜反应和水解反应。
(5)以CH3CHO为原料可合成Y,请结合本题信息,设计合成路线(无机试剂及溶剂任选)。
注:合成路线的书写格式参照如下示例流程图。CH3CH2OHH2C===CH2BrH2C—CH2Br
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期末化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列说法正确的是
A.若5.6 LN2中含有n个氮分子,则阿伏加德罗常数一定为4n
B.标准状况下,1L苯完全燃烧生成的气态产物的分子数为(6/22.4)NA
C.14 g乙烯和丙烯的混合气体中所含分子总数为0.5NA
D.0.1molC3H6Cl2中化学键总数为NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期末化学试卷(解析版) 题型:选择题
将2molA与2molB混合于2L的密闭容器中发生如下反应:2A(g)+3B(g) 2C(g)+zD(g),2s后A的转化率为50%,测得v(D)=0.25mol•L-1•s-1,下列推断不正确的是
2C(g)+zD(g),2s后A的转化率为50%,测得v(D)=0.25mol•L-1•s-1,下列推断不正确的是
A.v(C)=v(D)=0.25mol•L-1•s-1
B.C的体积分数为28.6%
C.B的转化率为25%
D.z=2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期末化学试卷(解析版) 题型:简答题
【加试题】工业制硫酸,利用催化氧化反应将SO2转化为SO3是一个关键步骤。请回答:
(1)某温度下,SO2(g)+O2(g) SO3(g) ;ΔH=-98 kJ · mol-1。开
SO3(g) ;ΔH=-98 kJ · mol-1。开 始时在100 L的密闭容器中加入4.0 mol
始时在100 L的密闭容器中加入4.0 mol SO2(g)和10.0 mol O2(g),当反应达到平衡时共放出热量196 kJ,该温度下平衡常数K=________ 。
SO2(g)和10.0 mol O2(g),当反应达到平衡时共放出热量196 kJ,该温度下平衡常数K=________ 。
(2)一定条件下,向一带活塞的密闭容器中充入2 mol SO2和1 mol O2,发生下列反应:2SO2(g)+O2(g) 2SO3(g),达到平衡后改变下述条件,SO2、O2、SO3气体平衡浓度都比原来增大的是________(填字母)。
2SO3(g),达到平衡后改变下述条件,SO2、O2、SO3气体平衡浓度都比原来增大的是________(填字母)。
A.保持温度和容器体积不变,充入2 mol SO3
B.保持温度和容器体积不变,充入2 mol N2
C.保持温度和容器体积不变,充入0.5 mol SO2和0.25 molO2
D.保持温度和容器内压强不变,充入1 mol SO3
E.升高温度
F.移动活塞压缩气体
(3)某人设想以下图所示装置用电化学原理生产硫酸,写出通入SO2的电极的电极反应式:______。

(4)下列关于2SO2(g)+O2(g) 2SO3(g)反应的图像中,
2SO3(g)反应的图像中, 一定正确的是________(填序号)。
一定正确的是________(填序号)。

(5)①某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示。当平衡状态由A变到B时,平衡常数K(A)_______ K(B)(填“>”、“<”或“=”)。
②将一定量的SO2(g)和O2(g)放入某固定体积的密闭容器中,在一定条件下,c(SO3)的变化如下图所示。若在第5分钟将容器的体积缩小一半后,在第8分钟达到新的平衡(此时SO3的浓度为0.25 mol·L-1)。请在下图画出此变化过程中SO3(g)浓度的变化曲线。

查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆哈密二中高二6月月考化学试卷(解析版) 题型:选择题
丙烷的分子结构可简写成键线式结构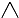 ,有
,有 机物A的键线式结构为
机物A的键线式结构为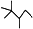 ,有机物B与等物质的量的H2发生加成反应可得到有机物A,下列有关说法错误的是( )
,有机物B与等物质的量的H2发生加成反应可得到有机物A,下列有关说法错误的是( )
A.有机物A的一氯代物只有4种
B.用系统命名法命名有机物A,名称为2,2,3-三甲基戊烷
C.有机物A的分子式为C8H18
D.B的结构可能有3种,其中一种的名称为3,4,4-三甲基-2-戊烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com