
日常所用的干电池其电极分别为碳棒(上面有铜帽)和锌皮,以糊状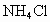 和
和 作为电解液(其中加入
作为电解液(其中加入 吸收
吸收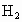 ),电极反应可简化为
),电极反应可简化为 ,
,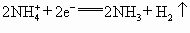 (
( 与
与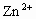 结合,)根据上述叙述判断以下正确的是
结合,)根据上述叙述判断以下正确的是
[ ]
A.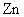 为正极,碳为负极
为正极,碳为负极
B.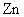 为负极,碳为正极
为负极,碳为正极
C.工作时电子由碳极经外电路流向锌极
D.长时间连续使用时内装的糊状物可能流出腐蚀所用的电器
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源:必修二训练化学苏教版 苏教版 题型:021
|
日常所用的干电池其电极分别为碳棒(上面有铜帽)和锌(皮),以糊状NH4Cl和ZnCl2作为电解质(其中加入MnO2吸收H2),电极反应可简化为:Zn-2e- | |
A. |
Zn为正极,碳为负极 |
B. |
Zn为负极,碳为正极 |
C. |
工作时电子由碳极经外电路流向锌极 |
D. |
长时间继续使用时内装的糊状物可能流出腐蚀所用的电器 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A.Zn为正极,碳为负极
B.Zn为负极,碳为正极
C.工作时电子由碳极经外电路流向锌极
D.长时间继续使用时内装的糊状物可能流出腐蚀所用的电器
查看答案和解析>>
科目:高中化学 来源:2014届福建省高二第一次月考化学试卷(解析版) 题型:选择题
日常所用的干电池的电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作电解质(其中加入MnO2氧化吸收H2), 电极反应可简化为:Zn-2e-==Zn2+;2NH4++2e- =NH3+H2,根据上述叙述判断下列说法正确的是 ( )
A. 干电池中锌为正极,碳为负极
B. 干电池工作时,电流由锌极经外电路流向碳极
C. 干电池长时间连续工作时,内装糊状物可能流出腐蚀用电器
D. 干电池可实现化学能向电能的转化和电能向化学能的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
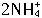 +2e-=2NH3↑+H2↑(NH3与Zn2+络合)。根据上面叙述判断下列结论正确的是( )。
+2e-=2NH3↑+H2↑(NH3与Zn2+络合)。根据上面叙述判断下列结论正确的是( )。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com