
| 组 分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数 | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |
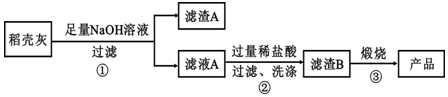
分析 Ⅰ、石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成,书写顺序是:活泼金属元素氧化物、较活泼金属元素氧化物、二氧化硅、水;
Ⅱ、稻壳灰用足量的氢氧化钠浸泡,过滤得A为硅酸钠、氢氧化钠、氢氧化钾、偏铝酸钠的混合溶液,滤渣A含有C以及氧化铁,A溶液中加入盐酸生成硅酸沉淀,过滤、洗涤得滤渣B为硅酸,煅烧硅酸可得二氧化硅,据此分析作答.
解答 解:Ⅰ、石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成,书写顺序是:活泼金属元素氧化物、较活泼金属元素氧化物、二氧化硅、水,所以为:CaO•3MgO•4SiO2;
故答案为:CaO•3MgO•4SiO2;
Ⅱ、(1)二氧化硅为酸性氧化物,氧化钠、氧化铁为碱性氧化物,氧化铝为两性氧化物,所以最多涉及3中氧化物,
故答案为:3;
(2)二氧化硅为酸性氧化物,与氢氧化钠反应生成硅酸钠和水,离子方程式为SiO2+2OH-=SiO32-+H2O,
故答案为:SiO2+2OH-=SiO32-+H2O;
(3)氧化钠、氧化钾均能与水反应生成可溶性碱,氧化铝为两性氧化物能够与强碱反应生成可溶性偏铝酸盐,二氧化硅 为酸性氧化物与氢氧化钠反应生成可溶性硅酸钠,三氧化二铁、碳与氢氧化钠不反应,所以过滤剩余的滤渣为C和Fe2O3,
故答案为:C和Fe2O3;
(4)沉淀的洗涤方法:向漏斗中注入蒸馏水致水浸没沉淀,让水自然流下后,再重复2-3次,
故答案为:往漏斗里的沉淀中注入蒸馏水致水浸没沉淀,让水自然流下,重复2-3次;
(5)硅酸不稳定受热易分解生成二氧化硅和水,其反应方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O;灼烧固体需要的仪器有:坩埚钳、酒精灯、三脚架、坩埚、泥三角,
故答案为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O;泥三角;坩埚钳.
点评 本题以硅及其化合物性质为载体考查物质的制备以及分离提纯,侧重于学生分析、实验能力的考查,解答本题时注意熟悉氧化物的分类,明确硅及其化合物性质,题目难度中等.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠不可露置在空气中,要密封保存 | |
| B. | 剩余的金属钠应放回原试剂瓶 | |
| C. | 氢氟酸应密封保存在玻璃瓶中 | |
| D. | 实验室保存FeCl2时常向其中加入铁屑 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发时,蒸发皿中固体不能蒸干才停止加热 | |
| B. | 蒸馏时,温度计水银球应靠近蒸馏烧瓶的支管口处 | |
| C. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 焰色反应时,用稀硫酸洗净铂丝,并在火焰上灼烧至无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
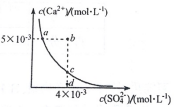 常温下,Ksp(CaSO4)=9 х 10?6,CaSO4 在水溶液中的沉淀溶解平衡曲线如图所示.下列说法不正确的是( )
常温下,Ksp(CaSO4)=9 х 10?6,CaSO4 在水溶液中的沉淀溶解平衡曲线如图所示.下列说法不正确的是( )| A. | b 点可能有沉淀生成 | |
| B. | a 点对应的Ksp 等于c 点对应的Ksp | |
| C. | 在d 点溶液中加入一定量的CaCl2可能会有沉淀析出 | |
| D. | CaSO4 溶解在水中,一定有c(Ca2+)=c(SO42-)=3×10-3mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.1g氯气与足量的氢氧化钠溶液反应转移的电子数为0.2×6.02×1023 | |
| B. | 50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| C. | 0.1molNa2O2与足量二氧化碳充分反应转移的电子数为0.2NA | |
| D. | 0.1molFe在0.1mol氯气中燃烧,转移的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 分类 | 名称(或俗名) | 化学式 | |
| A | 碱性氧化物 | 铁红 | FeO |
| B | 碱性氧化物 | 刚玉 | Al2O3 |
| C | 酸 | 硫酸 | H2S |
| D | 盐 | 纯碱 | Na2CO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用石墨棒做电极电解氯化铜溶液,与负极相连的石墨棒上有气泡产生 | |
| B. | 氢氧燃料电池工作时氢气在负极被氧化 | |
| C. | 铅蓄电池充电时,PbSO4仅在负极生成 | |
| D. | 红热的铁丝与冷水接触,表面形成蓝黑色保护层,这种变化属于原电池反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6 g Fe 和足量的氧气完全燃烧失去电子数为 3N A | |
| B. | 1L 浓度为 0.5mol/LFeCl3 溶液加热煮沸后,会生成 0.5molFe(OH)3胶体粒子 | |
| C. | 常温常压下,23 g NO2 和 N2O4 的混合气体一定含有 N A 个氧原子 | |
| D. | 标况下,4.48L 的水中含有 H2O 分子的数目为 0.2N A |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com