
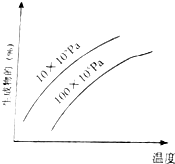
 由可逆反应测绘出图象如图,纵坐标为生成物在平衡混合物中的百分含量,下列对该反应的判断正确的是( )
由可逆反应测绘出图象如图,纵坐标为生成物在平衡混合物中的百分含量,下列对该反应的判断正确的是( )| A. | 反应物中一定有气体 | B. | 生成物中不一定有气体 | ||
| C. | 正反应一定是放热反应 | D. | 正反应一定是吸热反应 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是电子总数的$\frac{2}{3}$ |
| Z | 第三周期原子半径最小的金属 |
| A. | 气态氢化物的热稳定性:X>W | |
| B. | 最高价氧化物对应水化物的酸性:Y>X | |
| C. | 离子半径:Z>W | |
| D. | X在自然界中以游离态和化合态形式存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯能使溴水褪色 | |
| B. | 乙烯能使酸性高锰酸钾溶液褪色 | |
| C. | 将苯加入溴水中,因苯能与溴水发生加成反应而使溴水褪色 | |
| D. | 50~60℃时,在浓硫酸存在下,苯能与浓硝酸反应生成硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ⑧ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 4 | ⑨ |
 .
.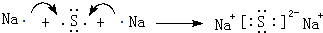 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
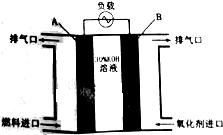 CO、H2、CH4、C2H5OH是常用的燃料,它们每1mol分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量依次为283.0kJ、285.8kJ、890.3kJ、1366.8kJ.
CO、H2、CH4、C2H5OH是常用的燃料,它们每1mol分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量依次为283.0kJ、285.8kJ、890.3kJ、1366.8kJ.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 实验室盛放碳酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞 | |
| B. | 泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,使用时只需将其混合就可产生大量二氧化碳的泡沫 | |
| C. | 将稀盐酸逐滴加入到Na2CO3溶液中,开始无二氧化碳放出 | |
| D. | 可用碳酸钠与醋酸制取少量二氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+、NO3-、NH4+ | B. | Na+、K+、CO32- | C. | Fe3+、S042-、Cl- | D. | CH3COO-、Na+、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
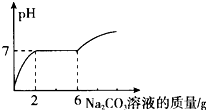 在烧杯中盛有10g HCl和BaCl2的混合溶液,向其中逐滴滴入溶质质量分数为13.25%的碳酸钠溶液.测得溶液pH与加入的碳酸钠溶液的质量关系如图所示.
在烧杯中盛有10g HCl和BaCl2的混合溶液,向其中逐滴滴入溶质质量分数为13.25%的碳酸钠溶液.测得溶液pH与加入的碳酸钠溶液的质量关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com