
| ||
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
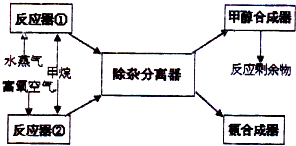 ij�������Լ���Ϊ��Ҫԭ������ȡ�ϳɼ״����ϳɰ���ԭ�ϣ�����Ҫ��ӦΪ��
ij�������Լ���Ϊ��Ҫԭ������ȡ�ϳɼ״����ϳɰ���ԭ�ϣ�����Ҫ��ӦΪ��| 2 |
| 3 |
| n(H2) |
| n(N2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1mol/L NaCl��Һ����NA��Na+ |
| B����״���£�22.4L H2O�к���NA��H2O���� |
| C�������£�22g CO2����NA����ԭ�� |
| D��2mol��������ϡ���ᷴӦ����3NA��H2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |

| �ı�ķ�Ӧ���� | ��Ӧ���ʸı�Ľ�� |
| ���ͷ�Ӧ��ϵ���¶� | |
| �������������Ϊ1L | |
| ʹ�ô��� | |
| ��������������䣬����һ��������������ѹǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ͭ����ķ�Ӧ�У�1molͭʧȥ�ĵ�����ΪNA |
| B����״���£�11.2LSO3������ԭ����Ϊ0.5NA |
| C����2H��18O����ɵ�ˮ11g������������������Ϊ4NA |
| D��1molCl2��������ˮ��Ӧ��ת�Ƶĵ�����Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Na2CO3��Һ��ϴ�Ӽ���CO-23+H2O?HCO-3+OH- | ||||
B��������������ˮ������Cl2+H2O
| ||||
| C����ⱥ��ʳ��ˮ���ռ2Cl-+2H2O�TCl2��+H2��+2OH- | ||||
| D��Fe2O3���ڹ�����������У�Fe2O3+6H+=2Fe3++3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Cu��ȥFeCl2��Һ��������FeCl3���ʣ�Cu+2Fe3+�TCu2++2Fe2+ |
| B����ҵ����NO2��ˮ��Ӧ��ȡHNO3��3NO2+H2O�TNO3-+NO+2H+ |
| C��������������Һ��ȥ�����������Ĥ��Al2O3+2OH-�T2AlO2-+H2O |
| D������ͭ��Һ������������Һ��Ӧ��Cu2++2OH-=Cu��OH��2�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com