
| A. | 臭氧空洞、温室效应、光化学烟雾、硝酸型酸雨的形成都与氮氧化合物有关 | |
| B. | 研制出性能优良的催化剂可使反应的温度降低,提高反应速率,从而起到很好的节能效果 | |
| C. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下△H 不同 | |
| D. | 光分解水制氢气、植物秸秆制沼气、高粱制乙醇都涉及到生物质能的利用 |
分析 A.温室效应与二氧化碳有关;
B.催化剂能够大幅度提高反应速率,可使反应的温度降低;
C.反应热与反应物和生成物的状态有关,与反应条件无关;
D.光分解水制氢气,把光能直接转化化学能.
解答 解:A.温室效应与二氧化碳有关,与氮氧化物无关,故A错误;
B.催化剂可以使反应温度降低,能加快反应速率,从而起到节能效果,故B正确;
C.反应热与反应物和生成物的状态有关,与反应条件无关,故C错误;
D.光分解水制氢气,把光能直接转化化学能,不涉及到生物质能的利用,故D错误;
故选:B.
点评 本题考查了能源的利用与环境保护,注意把握相关基础知识的理解,学习中要注意基础知识的积累,题目难度不大.


科目:高中化学 来源: 题型:解答题
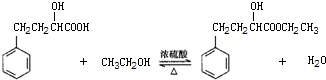
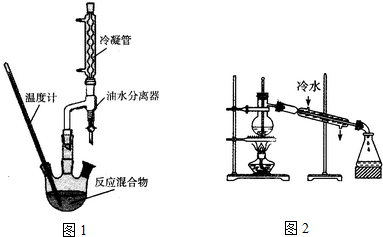
| 相对分子量 | 密度(g/cm3) | 沸点(℃) | 水溶性 | |
| 2-羟基-4-苯基丁酸 | 180 | 1.219 | 357 | 微溶 |
| 乙 醇 | 46 | 0.789 | 78.4 | 易溶 |
| 2-羟基-4-苯基丁酸乙酯 | 208 | 1.075 | 212 | 难溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将水加热,Kw增大,pH不变 | |
| B. | 向水中加入少量NaHSO4固体,溶液的c(H+)增大,水电离的c(H+)降低 | |
| C. | 向水中加入少量NaOH固体,平衡逆向移动,溶液的c(OH-)降低 | |
| D. | 向水中加入少量NH4Cl固体,平衡正向移动,溶液的c(OH-)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把碳棒放在酒精喷灯上灼烧 2-3min 后即投入到冷水中,重复操作几次,可制得多孔碳棒 | |
| B. | 在中和热的测定实验中,将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,立即读出并记录 溶液的起始温度,充分反应后再读出并记录反应体系的最高温度 | |
| C. | K2CrO4 溶液中存在平衡 2CrO${\;}_{4}^{2-}$+2H+Cr2O${\;}_{7}^{2-}$+H2O,加稀硝酸则溶液由黄色变为橙色 | |
| D. | 分光光度计可以用来测定某些化学反应的反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
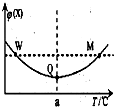 在某恒容密闭容器中充入一定量 X(g)和 Y(g),发生反应2X(g)+Y(g)?3Z(g)△H,反应过程中持续升高温度,测得混合体系中 X 的体积分数与温度的 关系如图.下列推断正确的是( )
在某恒容密闭容器中充入一定量 X(g)和 Y(g),发生反应2X(g)+Y(g)?3Z(g)△H,反应过程中持续升高温度,测得混合体系中 X 的体积分数与温度的 关系如图.下列推断正确的是( )| A. | M 点时,Y 的转化率最大 | |
| B. | 升高温度,平衡常数减小 | |
| C. | 平衡后充入 Z 达到新平衡时 Z 的体积分数增大 | |
| D. | W,M 两点 Y 的正反应速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F、G、H八种短周期元素,其单质的沸点如图所示.
A、B、C、D、E、F、G、H八种短周期元素,其单质的沸点如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4 | B. | CuSO4 | C. | HCl | D. | KCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com