
分析 氧化还原反应的特征是元素化合价的升降,如有元素化合价的变化,则属于氧化还原反应,结合分解反应和化合反应、置换反应的特点解答该题.
解答 解:A.2Na+2H2O═2NaOH+H2↑反应中Na、H元素的化合价发生变化属于氧化还原反应,还属于置换反应;
B.CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O,反应中C、O元素的化合价发生变化属于氧化还原反应,反应中有两种产物不是化合反应;
C.KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑反应中Cl、O元素的化合价发生变化属于氧化还原反应,反应物只有一种属于分解反应;
D.CaCO3+2HCl═CaCl2+H2O+CO2↑反应中没有元素化合价的变化,不是氧化还原反应;
E.Na2O+CO2═Na2CO3 反应中没有元素化合价的变化,不是氧化还原反应;
F.CO2+C$\frac{\underline{\;点燃\;}}{\;}$2CO反应中C元素的化合价发生变化属于氧化还原反应,两种反应物生成一种物质,属于化合反应;
既属于化合反应又属于氧化还原反应的有F,不属于氧化还原反应的有E;
故答案为:F;DE.
点评 本题考查氧化还原反应,侧重于学生的分析能力考查,注意从元素化合价的角度认识氧化还原反应的相关概念和物质的性质,把握物质的反应类型的判断,难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容量瓶:500mL、250mL各一个;CuSO4:共120g | |
| B. | 容量瓶:750mL;CuSO4:120g | |
| C. | 容量瓶:1000mL;CuSO4•5H2O:160g | |
| D. | 容量瓶:1000mL;CuSO4:160g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 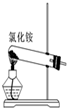 实验室用如图装置制取氨气 | |
| B. |  装置可用于制备氢氧化亚铁并观察其颜色 | |
| C. | 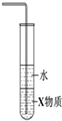 如图装置中X若为四氯化碳,可用于吸收氨气,并防止倒吸 | |
| D. | 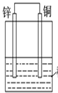 如图装置是原电池,锌电极为负极,发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 (1)实验室常用装置E制备Cl2,写出该反应的离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
(1)实验室常用装置E制备Cl2,写出该反应的离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铯的碱性非常强 | |
| B. | 碱金属单质中铯的沸点最低 | |
| C. | 将一小块铯投入水中,实验现象与钠和水反应的完全相同 | |
| D. | 铯可以与很多非金属反应,形成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合成纤维和光导纤维都属于新型无机非金属材料 | |
| B. | “地沟油”禁止食用,但经过加T处理后,可以用来制取肥皂和生物柴油 | |
| C. | 大力推广应用“脱硫、脱硝”技术,可减少硫氧化物、氮氧化物对空气的污染 | |
| D. | 2015年10月我国科学家屠呦呦获诺贝尔医学、生理学奖,她发现、创制的药物青篙素( )是治疗疟疾的特效药,青篙素的分子式为C15H22O5 )是治疗疟疾的特效药,青篙素的分子式为C15H22O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
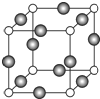 已知 A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素.E是第四周期的p区元素且最外层只有2对成对电子,F元素原子序数为29.
已知 A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素.E是第四周期的p区元素且最外层只有2对成对电子,F元素原子序数为29.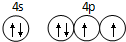 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com