
一种离子与多种酸根离子构成的盐称为“混盐”,如氯化硝酸钙[Ca(NO3)Cl];而“复盐”则是指含有多种简单阳离子和一种酸根阴离子的盐,如KAl(SO4)2。据此,下列各化合物中属于混盐的是
| A.(NH4)2Fe(SO4) | B.BiONO3 | C.CaOCl2 | D.K3[Fe(CN)6] |
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源:2013-2014广西贵港市毕业班5月高考冲刺模拟理综化学试卷(解析版) 题型:选择题
下列离子方程式表达正确的是
A.碘化亚铁溶液中通入少量氯气:Cl2+2Fe2+=2Fe3++2Cl—
B.向1mol/L 0.1L的明矾溶液中加入0.5mol/L 0.2L的Ba(OH)2溶液:
2Al3++3SO42—+ 3Ba2++6OH—=2Al(OH)3↓+3BaSO4↓
C.将蛋壳浸泡到醋酸中:CO32—+2CH3COOH=2CH3COO—+ CO2↑+H2O
D.将过氧化钠与水反应:2O22—+2H2O=O2+4OH—
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据“绿色化学”的思想,某化学家设计了下列化学反应步骤:
该方案的相关叙述正确的是
| A.该实验的目的是制取HBr | B.该过程的副产品是Hg |
| C.该过程得到的气体只有H2 | D.该过程的本质是水的分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应属于氧化还原反应的是 ( )
| A.CaCO3+2HCl===CaCl2+CO2↑+H2O | B.CO2+H2O===H2CO3 |
| C.2H2O2催化剂 2H2O+O2↑ | D.CaCO3 CaO+CO2↑ CaO+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
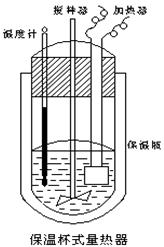
(共14分)(Ⅰ)某化学实验小组为确定过氧化氢分解的最佳催化条件,用如图装置进行实验,反应物用量和反应停止的时间数据如下表:
 MnO2 MnO2时间 H2O2 | 0.1 g | 0.3 g | 0.8 g |
| 10 mL 1.5% | 223 s | 67 s | 56 s |
| 10 mL 3.0% | 308 s | 109 s | 98 s |
| 10 mL 4.5% | 395 s | 149 s | 116 s |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
(16分)以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:
(1)酸溶过程中Fe2O3与稀硫酸反应的化学方程式为 ;
“滤渣A”主要成份的化学式为 。
(2)还原过程中加入FeS2的目的是将溶液中的Fe3 +还原为Fe2 +,而本身被氧化为H2SO4,请完成该反应的离子方程式:FeS2 + 14Fe3 + + H2O="=" 15Fe2 + + SO42- + 。
(3)氧化过程中,O2、NaOH与Fe2+反应的离子方程式为 。
(4)为了确保铁红的质量,氧化过程需要调节溶液的pH的范围是 (几种离子沉淀的pH见下表);滤液B可以回收的物质有(写化学式) 。
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com